ORDIN Nr. 1577
din 16 septembrie 2008
pentru aprobarea Normelor
metodologice de implementare a Programului national de control al tuberculozei
ACT EMIS DE:
MINISTERUL SANATATII
ACT PUBLICAT IN:
MONITORUL OFICIAL NR. 766 din 13 noiembrie 2008
Având în vedere prevederile Legii nr. 95/2006 privind
reforma în domeniul sănătăţii, cu modificările şi
completările ulterioare,
văzând Referatul de aprobare al Autorităţii de Sănătate
Publică şi Agenţiei Naţionale de Programe din Ministerul Sănătăţii Publice nr.
E.N. 9.661 din 16 septembrie 2008,
în temeiul prevederilor Hotărârii Guvernului nr.
862/2006 privind organizarea şi funcţionarea Ministerului Sănătăţii Publice, cu
modificările şi completările ulterioare,
ministrul sănătăţii publice emite următorul ordin:
Art. 1. - Se aprobă Normele metodologice de
implementare a Programului naţional de control al tuberculozei, prevăzute în
anexa care face parte integrantă din prezentul ordin.
Art. 2. - Structurile din Ministerul Sănătăţii Publice,
autorităţile de sănătate publică judeţene şi a municipiului Bucureşti, precum şi toţi furnizorii de servicii medicale vor duce la îndeplinire prevederile
prezentul ordin.
Art. 3. - Prezentul ordin se publică în Monitorul
Oficial al României, Partea I.
Ministrul sănătăţii publice,
Gheorghe Eugen Nicolăescu
ANEXĂ
NORME METODOLOGICE
de implementare a
Programului naţional de control al tuberculozei
ABREVIERI
AE -anchetă epidemiologică
ANP -Agenţia Naţională de Programe
ASP-MSP -Autoritatea de Sănătate Publică din
Ministerul Sănătăţii Publice
ASPJ - autoritatea de sănătate
publică judeţeană/a municipiului Bucureşti
BAAR - bacili acid-alcoolo-rezistenţi
bK - bacil Koch
CAM - centrul de asistenţă medicală
CASJ - casa
de asigurări de sănătate judeţeană/a municipiului Bucureşti
CERCM - comisia de expertiză şi recuperare
a capacităţii de muncă
CMI - cabinet medical individual
CNAS - Casa Naţională de Asigurări de
Sănătate
CPAIC - Comisia de Pneumologie,
Alergologie şi Imunologie Clinică
CRR - Crucea Roşie Română
CTJ - coordonator tehnic judeţean
CTN - coordonator tehnic naţional
DOT -
tratament sub directă observare
DOTS - tratament sub directă
observare, de scurtă durată
DOTS plus - procurarea, asigurarea şi
distribuţia medicamentelor antituberculoase de linia a II-a pentru MDR-TB
DPF - dispensarul de
pneumoftiziologie
ECDC - Centrul European pentru
Prevenirea şi Controlul Bolilor Transmisibile
GFATM - Fondul Global de Luptă împotriva
HIV/SIDA, Tuberculozei şi
Malariei
GLC - Green Light Committee
IEC - informare-educare-comunicare
IGRA - metodă de detecţie moleculară
rapidă a infecţiei TB
INPMN - Institutul Naţional de
Pneumoftiziologie „Prof. dr. Marius Nasta" Bucureşti
LNR - laborator naţional de
referinţă
LRR - laborator regional de
referinţă
MA -Ministerul Apărării
MDG - Millenium Developement Goals
MDR-TB - tuberculoză
cu microorganisme rezistente cel puţin la HIN şi RMP
MF - medic de familie
MIRA - Ministerul Internelor şi
Reformei Administrative
MJ - Ministerul Justiţiei
MP - morfopatologie
MSP - Ministerul Sănătăţii Publice
MT - Mycobacterium
tuberculosis
OMS - Organizaţia Mondială a
Sănătăţii
ONU - Organizaţia Naţiunilor Unite
PCR -
reacţie de polimerizare în lanţ (Polimerase Chain
Reaction)
PNCT - Programul naţional de control
al TB
PPD - Protein Purified
Derivative
RAI - riscul anual de infecţie
TB -
tuberculoză
UC - Unitatea centrală a
softului de colectare a datelor privind TB
UCM - Unitatea centrală de
management
UE -Uniunea Europeană
UJ -
unitatea judeţeană a softului de colectare a datelor privind TB
XDR-TB - tuberculoză cu rezistenţă
extinsă la medicamentele antituberculoase
INTRODUCERE
In România, MSP consideră că TB constituie o problemă
majoră de sănătate publică şi, ca urmare, activităţile antituberculoase
prevăzute în PNCT - diagnosticul şi tratamentul bolnavilor de TB, controlul
contacţilor acestora, tratamentul preventiv, activităţile de informare, educare
şi comunicare - sunt gratuite.
In România, strategia DOTS
recomandată de OMS pentru controlul TB are o acoperire de 100% din anul 2005.
Documentul de faţă a fost elaborat pe baza strategiilor şi documentelor în
domeniul controlului TB recomandate de OMS.
ORGANIZAREA PNCT
Răspunsul sistemului de sănătate din România pentru
reducerea poverii TB se desfăşoară conform Strategiei naţionale de control al
TB 2006-2010 şi este realizat prin PNCT, constituit prin coroborarea
subprogramului „Supravegherea şi controlul tuberculozei" cu subprogramul
„Tratamentul bolnavilor cu tuberculoză", în conformitate cu hotărârile
anuale pentru definirea programelor naţionale de sănătate implementate de
MSPşiCNAS.
PNCT este coordonat din punct de vedere tehnic de INPMN,
beneficiind de consilierea de specialitate a CPAIC a MSP.
Funcţionarea PNCT este
asigurată de o structură organizată ierarhic pe 3 niveluri, fiecare nivel având
atribuţii şi relaţii funcţionale bine stabilite.
Primul nivel este
constituit din reţeaua de asistenţă medicală primară (MF/medici de medicină
generală) care asigură identificarea suspecţilor şi a contacţilor de TB şi care
aplică tratamentul bolnavilor sub directă observare, în faza de continuare, prescris de medicii
pneumologi din reţeaua de pneumoftiziologie a MSP şi a celorlalte ministere cu
reţele proprii de servicii de sănătate.
Reţeaua de asistenţă medicală primară:
- identifică suspecţii şi contacţii de TB;
- administrează medicaţia antituberculoasă sub directă
observare;
- participă la efectuarea AE.
Al doilea nivel este
reprezentat de:
- DPF teritoriale şi ale
sectoarelor municipiului Bucureşti (al căror număr variază între 2 şi 8 în
fiecare judeţ);
- reţeaua de laboratoare de bacteriologie bK;
- unităţile sanitare cu paturi: secţiile de
pneumoftiziologie şi spitalele de pneumoftiziologie;
- epidemiologul judeţean de la
nivelul ASPJ;
- CTJ al PNCT.
Unităţile din al doilea nivel sunt prevăzute în anexele
nr. 2a), 2b) şi 2c), care fac parte integrantă din prezentele norme
metodologice.
DPF este încadrat cu un
număr variabil de medici pneumologi şi de cadre medii sanitare şi deserveşte un
teritoriu cu o populaţie de aproximativ 100.000 de locuitori. DPF este responsabil
pentru aplicarea şi monitorizarea PNCT în teritoriul arondat: asigură
diagnosticul, tratamentul, înregistrarea, raportarea şi monitorizarea cazurilor
de TB, precum şi controlul transmiterii infecţiei TB prin participarea la
efectuarea AE. In acest scop colaborează cu MF şi supervizează activitatea
acestora în depistarea TB şi administrarea tratamentului sub directa observare,
iar în efectuarea AE colaborează atât cu MF, cât şi cu medicul epidemiolog al teritoriului respectiv,
responsabil de implementarea PNCT.
DPF sunt coordonate de un medic coordonator, numit din
rândul medicilor încadraţi în unitatea respectivă de către CTJ al PNCT şi
aprobat de către ASPJ. Fişa postului coordonatorului DPF teritorial este
prezentată în anexa nr. 1, care face parte integrantă din prezentele norme
metodologice.
Unităţile cu paturi asigură
diagnosticul şi tratamentul pacienţilor cu TB, precum şi izolarea cazurilor
infecţioase până la negativarea acestora. Medicii din spitale şi secţii
colaborează cu cei din DPF prin anunţarea obligatorie, în termen de 48 de ore,
a existenţei unui caz de TB sau MDR-TB în teritoriul arondat DPF respectiv,
precum şi prin transmiterea documentaţiei medicale la externarea pacientului şi
a rezultatelor de laborator care sunt finalizate şi primite ulterior
externării. Spitalele, secţiile şi cabinetele de alte specialităţi, precum şi
cabinetele de pneumologie, inclusiv cele private, care depistează cazuri de TB
sau MDR-TB cu localizare pulmonară sau extrapulmonară au aceleaşi obligaţii cu cele
descrise mai sus.
Orice caz de MDR-TB sau XDR-TB nou-diagnosticat este
anunţat în termen de 48 de ore CTJ al PNCT, centrului de excelenţă la care este
arondat teritorial, precum şi Unităţii de supraveghere epidemiologică a
tuberculozei de la INPMN.
Tratamentul TB este gratuit pentru toţi bolnavii, iar
medicamentele antituberculoase sunt furnizate atât pentru spitale, cât şi
pentru DPF, prin 190 de farmacii cu circuit închis.
Pentru îngrijirea pacienţilor cu MDR/XDR-TB
funcţionează două centre de excelenţă în Bucureşti şi la Bisericani (judeţul
Neamţ). Aceste două centre au fost înfiinţate cu aprobarea GLC, beneficiind de
finanţarea GFATM. Aceste centre de excelenţă pot îngriji anual 200 de cazuri de
MDR/XDR-TB. Pacienţii care urmează să fie internaţi în aceste centre de
excelenţă trebuie să fie de acord să urmeze în regim DOT tratamentul prescris
pe toată durata acestuia.
Vor fi asigurate măsuri pentru utilizarea cu eficienţă
maximă a celor două centre de excelenţă, în sensul utilizării paturilor
disponibile la capacitate maximă.
Pe lângă fiecare centru de excelenţă funcţionează o
comisie MDR-TB, formată din medici specialişti pneumologi cu autoritate
profesională înaltă, care analizează îndeplinirea criteriilor de internare a
bolnavilor în aceste centre. Ceilalţi pacienţi diagnosticaţi cu MDR/XDR-TB
beneficiază şi ei de analiza comisiei şi de scheme similare de tratament ca şi
cei admişi în centrele de excelenţă, numai că vor fi asistaţi în celelalte
unităţi ale PNCT.
Reţeaua de laboratoare de bacteriologie bK: în România există laboratoare de bacteriologie bK între care există
relaţii de interdependenţă, toate contribuind la realizarea obiectivelor PNCT.
Existenţa reţelei laboratoarelor permite:
• aplicarea tehnicilor standardizate la nivelul
întregii ţări;
• asigurarea unor investigaţii speciale disponibile
numai în laboratoare specializate (de exemplu: testarea sensibilităţii la
substanţele antituberculoase, identificarea speciilor
de micobacterii);
• obţinerea informaţiilor necesare planificării şi
evaluării activităţii la toate nivelurile;
• obţinerea informaţiilor privind activitatea de
diagnostic şi identificarea eventualelor deficienţe, cu corectarea lor;
• aprecierea tendinţei confirmărilor bacteriologice,
creşterea procentului confirmărilor bacteriologice ale cazurilor constituind
cel mai bun indicator operaţional pentru un program de control al TB eficient.
Clasificarea laboratoarelor în funcţie de gradul de competenţă şi de complexitatea activităţilor:
1. laborator de nivel I - de
bază:
- asigură detectarea cazurilor prin examen microscopic;
- oferă informaţii epidemiologice privind profilul de
sănătate al comunităţii;
2. laborator de nivel II - intermediar:
- asigură efectuarea de examene microscopice pentru
evidenţierea BAARşi cultura micobacteriilor;
- trimite cultura pentru validare şi identificarea
micobacteriilor din complexul MT la laboratorul de nivel III;
3. laborator de nivel III:
- asigură efectuarea de examene microscopice pentru
evidenţierea BAAR, cultura cu identificarea micobacteriilor din complexul MT şi
antibiograma acestora pentru Rifampicină şi Izoniazidă. La acest nivel există 8
LRR (Iaşi, Cluj-Napoca, Buzău, Colibaşi, Craiova, Bucureşti - INPMN, Deva,
Braşov). Cele 8 LRR coordonează activitatea din câte 4-7 laboratoare judeţene
arondate şi din municipiul Bucureşti;
4. LNR din cadrul INPMN constituie nivelul la care se
realizează coordonarea, planificarea, organizarea, monitorizarea şi evaluarea
reţelei. Aici este instruit personalul cu studii superioare din laboratoarele
judeţene. Desfăşoară activitate de supervizare, asigurare a calităţii, de
informare şi management al resurselor.
Management şi supervizare a activităţii
laboratoarelor bK
Laboratoarele teritoriale bK sunt monitorizate şi
supervizate de laboratorul judeţean bK.
Laboratoarele judeţene bK sunt monitorizate şi
supervizate de laboratorul regional bK la care sunt arondate laboratoarele
judeţene, conform anexei nr. 2a).
Laboratoarele regionale bK sunt
monitorizate şi supervizate de către LNR.
Laboratoarele teritoriale bK sunt coordonate de către
un medic sau biolog coordonator desemnat de către coordonatorul judeţean pentru
laboratoarele bK şi aprobat de către ASPJ.
Laboratorul judeţean, regional şi al LNR sunt
coordonate de un medic sau biolog coordonator, desemnat de către coordonatorul
Grupului de lucru laboratoare de pe lângă UCM a PNCT şi aprobat de către
ASP-MSP.
Fişa postului coordonatorului laboratorului bK este
prevăzută în anexa nr. 3b), care face parte integrantă din prezentele norme
metodologice.
Laboratoarele de bacteriologie bK sunt în relaţie funcţională atât cu unităţile ambulatorii şi
spitaliceşti, cât şi între ele, prin transmiterea produselor biologice sau a
culturilor la laboratorul de nivel superior pentru continuarea investigaţiei,
validarea rezultatului obţinut şi pentru asigurarea controlului extern al
calităţii.
Structura reţelei de laboratoare bK din România este redată în anexa nr. 2a).
CTJ al PNCT este medic
de specialitate pneumologie nominalizat de către CTN al PNCT, cu aprobarea
ASP-MSP. CTJ asigură aplicarea PNCT în teritoriul judeţului respectiv.
Fişa postului CTJ al PNCT este prezentată în anexa nr.
3a), care face parte integrantă din prezentele norme metodologice.
Epidemiologul de la nivelul ASPJ cu responsabilităţi în derularea PNCT este desemnat de către
directorul executiv adjunct de sănătate publică şi are următoarele atribuţii
specifice:
- supravegherea epidemiologică;
- controlul focarelor de TB;
- evaluarea endemiei prin TB în teritoriu;
- controlul respectării normelor de prevenire a
infecţiilor nosocomiale în unităţile de pneumoftiziologie, în colaborare cu
medicul CTJ al PNCT.
CTJ şi epidemiologul de la nivelul ASPJ cu
responsabilităţi în derularea PNCT se află în relaţii de colaborare şi
acţionează împreună pentru supravegherea epidemiologica a infecţiei
tuberculoase în judeţul respectiv.
Alte structuri implicate în controlul TB
MJ, MA şi MIRA au în cadrul reţelelor proprii de
servicii de sănătate şi secţii de pneumoftiziologie. Aceste secţii au aceleaşi
responsabilităţi în aplicarea PNCT ca şi cele ale MSP. In plus, în lipsa DPF,
secţiilor respective le revin şi atribuţiile DPF ale MSP.
In cadrul reţelei de asistenţă medicală a MA şi MIRA
funcţionează atât unităţi cu paturi, cât şi ambulatorii, încadrate cu medici
pneumologi care asigură activităţi de control al TB pentru angajaţii
ministerelor respective şi pacienţii MF din reţeaua MAşi MIRA. Pentru
completarea investigaţiilor, aceştia sunt trimişi la unităţile de specialitate
ale MSP.
Cele 3 ministere cu servicii de sănătate proprii au şi
propriile unităţi cu atribuţii similare unităţilor de nivel I şi II ale PNCT.
Pentru MJ, echivalentul nivelului II este Departamentul
medical din cadrul Administraţiei Naţionale a Penitenciarelor, pentru MA,
Secţia de pneumoftiziologie a Spitalului Militar Central, iar pentru MIRA,
cabinetul de pneumoftiziologie din cadrul ambulatoriului Spitalului Militar de
Urgenţă „Prof. dr. Dimitrie Gerota".
In situaţia specială a îngrijirii cazurilor de TB
asociate cu infecţia HIV, medicii pneumologi colaborează cu specialiştii din
centrul regional HIV/SIDA unde sunt înregistraţi pacienţii.
Al treilea nivel este
reprezentat de:
- INPMN, care îşi desemnează prin regulamentul intern
de organizare şi funcţionare structurile responsabile;
- Comisia de supervizare a PNCT;
- Grupul de lucru pentru laboratoare.
Componenţa Comisiei de supervizare a PNCT şi cea a
Grupului de lucru pentru laboratoare sunt nominalizate prin ordin al
ministrului sănătăţii publice, la propunerea CTN al PNCT.
INPMN, ca for metodologic:
- coordonează din punct de vedere tehnic implementarea
PNCT;
- elaborează norme tehnice pentru medicii specialişti,
personalul de laborator, asistenţii medicali etc;
- monitorizează implementarea prevederilor PNCT;
- realizează legătura dintre principalii parteneri
implicaţi în activităţile de control al TB.
Instituţiile cu responsabilităţi în implementarea
PNCT şi atribuţiile acestora sunt următoarele:
• MSP: 1.ASP-MSP:
- aprobă componenţa Comisiei de supervizare a PNCT şi a
Grupului de lucru pentru laboratoare, precum şi CTJ ai PNCT;
- colaborează cu ANP pentru proiectarea anuală a PNCT;
2.ANP:
- coordonează elaborarea şi implementarea PNCT la nivel
naţional;
- răspunde de asigurarea, urmărirea, evidenţierea şi
controlul utilizării fondurilor aprobate pentru subprogramul „Supravegherea şi
controlul tuberculozei";
- monitorizează, controlează şi analizează indicatorii
fizici şi de eficienţă pentru subprogramul „Supravegherea şi controlul
tuberculozei";
3. CPAIC:
- participă la elaborarea strategiilor în domeniu;
- răspunde cu expertiză de specialitate oricăror
solicitări ale MSP în ceea ce priveşte modul de derulare şi rezultatele PNCT;
• CNAS:
- răspunde de asigurarea,
urmărirea, evidenţierea şi controlul utilizării fondurilor aprobate pentru
subprogramul „Tratamentul bolnavilor cu tuberculoză";
- monitorizează, controlează şi analizează indicatorii
fizici şi de eficienţă pentru subprogramul „Tratamentul bolnavilor cu
tuberculoză";
- colaborează cu comisia de experţi pentru subprogramul
„Tratamentul bolnavilor cu tuberculoză", care funcţionează pe lângă CNAS;
• CASJ:
- răspunde de asigurarea, urmărirea şi controlul
utilizării fondurilor alocate pentru subprogramul „Tratamentul bolnavilor cu
tuberculoză";
- analizează şi monitorizează indicatorii fizici şi de
eficienţă pentru subprogramul „Tratamentul bolnavilor cu tuberculoză",
transmişi de unităţile sanitare;
- încheie contracte cu unităţile sanitare prin care se
derulează subprogramul „Tratamentul bolnavilor cu tuberculoză";
• ASPJ:
- gestionează fondurile alocate derulării activităţilor
subprogramului „Supravegherea şi controlul tuberculozei";
- monitorizează utilizarea resurselor financiare
alocate PNCT la nivel judeţean;
- asigură derularea PNCT prin colaborarea dintre
coordonatorii de programe ai ASPJ şi CTJ al PNCT (medicul pneumolog);
• alte ministere:
- MA- prin reţeaua sanitară proprie - asigură
integrarea în PNCT;
- MIRA - prin reţeaua sanitară
proprie - asigură integrarea în PNCT;
- MJ - prin reţeaua sanitară proprie - asigură
integrarea în PNCT;
- Ministerul Educaţiei, Cercetării şi Tineretului -
este implicat în activităţile de IEC;
• organizaţii neguvernamentale: derulează proiecte conexe PNCT.
SCOPUL Şl OBIECTIVELE PNCT 2007-2011
Scopul PNCT este reprezentat de îmbunătăţirea stării de
sănătate a populaţiei României prin limitarea răspândirii infecţiei şi bolii
tuberculoase în rândul populaţiei.
Obiectivele PNCT până în 2011 sunt:
• acoperirea cu DOT a 100% din pacienţii diagnosticaţi
cu TB;
• menţinerea ratei de depistare a TB la nivelul de
peste 70%;
• atingerea şi menţinerea ratei de succes de 85%
pentru cazurile de TB pulmonară confirmate bacteriologic;
• scăderea ratei mortalităţii prin TB la 8%ooo.
DEPISTAREA TB
Depistarea prin simptome a TB - cunoscută şi sub numele de depistare pasivă - este o
activitate ce revine atât medicilor din reţeaua de asistenţă medicală primară,
cât şi celor de diverse alte specialităţi.
Pacienţii care vin din proprie
iniţiativă la medic şi care prezintă tuse seacă sau slab productivă, însoţită
de subfebrilitate, astenie fizică, inapetenţă, paloare, transpiraţii nocturne,
insomnie, nervozitate, scădere ponderală, simptome cu o vechime de 2-3
săptămâni, trebuie consideraţi ca potenţiali bolnavi de TB; în aceste cazuri se
recomandă dirijarea către DPF teritoriale sau secţia/spitalul de
pneumoftiziologie, după caz,
unde vor fi investigaţi pentru precizarea diagnosticului (vezi mai jos).
Orice persoană cu simptome
sugestive pentru diagnosticul de TB trebuie să se adreseze MF sau medicului
specialist din DPF. MF trimite pacientul suspect la DPF sau secţia/spitalul de
pneumoftiziologie, după caz.
Dacă în urma investigaţiilor diagnosticul de TB
pulmonară se confirmă, medicul pneumolog din secţia/spitalul de
pneumoftiziologie trebuie să anunţe în termen de 48 de ore DPF în teritoriul
căruia bolnavul are domiciliul real, declarat (indiferent de adresa sa legală,
înscrisă în documentele de identitate), completând fişa de anunţare a cazului
de TB.
Medicul pneumolog din DPF teritorial va informa, prin
scrisoare medicală, atât MF, cât şi medicul epidemiolog/de sănătate publică
asupra apariţiei cazului de îmbolnăvire cu TB, în vederea declanşării AE, în
termen de 3 zile de la primirea fişei de anunţare sau de la depistarea cazului.
Depistarea intensivă în
vederea diagnosticului precoce al TB constă în identificarea suspecţilor prin
control clinic repetat, urmată de evaluarea acestora prin examen bacteriologic
al sputei pentru bK şi examen radiologie; este responsabilitatea serviciilor de
asistenţă medicală primară, a medicilor din cabinetele şcolare, a medicilor
care asigură supravegherea stării de sănătate a angajaţilor, a medicilor
specialişti care au în îngrijire grupuri cu risc pentru TB, reţeaua de asistenţi
comunitari, mediatori sanitari etc. Depistarea intensivă se adresează
următoarelor grupuri vulnerabile la TB:
1. pauperii extremi, persoanele fără adăpost, asistaţii
social;
2. infectaţii HIV;
3. utilizatorii de droguri;
4. populaţia din penitenciare/alte instituţii
corecţionale;
5. persoanele spitalizate cronic în unităţi de
psihiatrie;
6. cazurile de neoplasm, diabet zaharat, hepatită
cronică sau ciroză cu virus B ori C, cu tratamente specifice;
7. persoanele care urmează
tratamente imunosupresive pentru diverse afecţiuni, persoanele cu transplanturi
de organe si colagenoze tratate cu imundepresoare (de exemplu, anti-TNF alfa);
8. etilicii cronici;
9. personalul care lucrează în unităţile sanitare;
10. muncitorii expuşi noxelor coniotice/cu pneumoconioze,
cei de pe şantiere de construcţii, cei cazaţi în dormitoare comune, navetiştii;
11. contacţii bolnavilor de TB;
12. persoanele din cămine de bătrâni, din
cămine-spital;
13. pacienţii hemodializaţi.
Selectarea persoanelor care trebuie examinate, precum
şi ritmicitatea acestor controale se fac în funcţie de gradul de risc, prin
colaborare între MF, medicii care îngrijesc aceste categorii vulnerabile şi
medicii pneumologi din DPF teritoriale.
DIAGNOSTICUL TB
A. Diagnosticul TB pulmonare
Diagnosticul clinic: unii
pacienţi (20-40% din cazuri) sunt asimptomatici, dar în majoritatea cazurilor
pacienţii prezintă cel puţin unu sau două simptome care îi determină să caute
asistenţa medicală: cel mai comun simptom este tusea (95% din cazuri), care
durează cel puţin 3 săptămâni; alte semne: pierdere ponderală, astenie, febră,
transpiraţii nocturne, dureri toracice, dispnee, hemoptizie.
Diagnosticul bacteriologic este singurul patognomonic, care stabileşte diagnosticul pozitiv al
TB. Este efectuat în majoritatea cazurilor din sputa expectorată spontan, dar
se pot folosi şi alte produse patologice.
Examinarea bacteriologică este metoda care asigură
diagnosticul de certitudine al TB.
Examenul direct al frotiului de
spută utilizând metoda de colorare Ziehl-Neelsen este esenţial în controlul TB
pentru că ajută la identificarea bolnavilor cu contagiozitate ridicată; un
număr mare de BAAR pe frotiu indică un număr mare de bacili expectoraţi.
Rezultatul este pozitiv dacă sputa conţine mai mult de 5.000 bacili/ml. Sensibilitatea
mică a metodei (22-40%) poate fi ameliorată prin examinarea de eşantioane
multiple.
Cultivarea micobacteriilor din spută este o metodă cu
sensibilitate mai mare pentru confirmarea diagnosticului de TB (rezultat
pozitiv dacă sputa conţine mai mult de 50 bacili/ml). Creşte cu până la 25%
numărul cazurilor de TB confirmată bacteriologic. Se efectuează în laboratoare
specializate.
După identificarea MTse poate efectua testarea
sensibilităţii la medicamentele anti TB cu scopul depistării tulpinilor bacteriene
rezistente.
In măsura asigurării finanţării corespunzătoare se
preconizează efectuarea testării sensibilităţii tuturor tulpinilor izolate la
medicamentele anti TB de linia I (HR pentru cazurile
noi).
Testele de sensibilitate sunt obligatorii pentru
toate cazurile în care se reiau tratamentele.
Recoltarea sputei de la suspecţii de TB este esenţială
pentru stabilirea diagnosticului.
Se recoltează întotdeauna 3 probe de spută separate,
chiar şi la acei suspecţi la care examenul radiologie pulmonar este normal.
Randamentul investigaţiei bacteriologice este
condiţionat de calitatea probelor de spută recoltate.
Probele de spută se recoltează în două zile succesive
de evaluare clinică, pentru a reduce numărul de vizite ale pacientului; două
probe de spută sunt recoltate în cursul vizitelor pacientului la dispensar, sub
supravegherea directă a unui lucrător sanitar, iar a treia probă este recoltată
de către pacient la domiciliu, dimineaţa devreme, înainte de a mânca, după ce
s-a spălat pe dinţi.
După recoltarea sputei se va completa Formularul pentru
solicitare/raportare examen bacteriologic pentru tuberculoză (anexa nr. 4, care
face parte integrantă din prezentele norme metodologice).
Sputa de bună calitate:
• este frecvent vâscoasă şi mucoidă;
• poate fi fluidă, dar cu fragmente de ţesut necrozat;
şi/sau
• poate fi stratificată în culori de la alb mat la
verde. Pentru detalii privind recoltarea sputei se va consulta anexa nr. 5, care face parte integrantă din prezentele norme metodologice.
In cazul în care primele 3 probe recoltate sunt
negative la examenul microscopic, se repetă recoltarea şi examinarea
bacteriologică în aceleaşi condiţii.
Examenul radiologie este metoda utilizată frecvent
pentru diagnosticul TB pulmonare. El are o sensibilitate înaltă, dar
specificitate joasă.
Modificările radiologice sunt utilizate ca argumente
pentru diagnosticul TB pulmonare neconfirmate bacteriologic.
In laboratorul de bacteriologie bK se efectuează,
pentru majoritatea cazurilor suspecte de TB, examenul
microscopic (M) şi cultura (C).
Examenul microscopic:
• decelează BAAR în spută. O concentraţie mare de
bacili în spută înseamnă implicit un număr mare de bacili expectoraţi;
• este o metodă rapidă, ieftină, care decelează cele
mai contagioase cazuri ce prezintă cel mai mare risc pentru persoanele din jur;
• are sensibilitate redusă;
• decelarea BAAR în examenul microscopic direct nu
înseamnă neapărat identificarea MT
Cultivarea MT:
• cultura pozitivă, urmată de identificarea MT, este
testul de confirmare a cazului. Cultivarea MT necesită 4-6 săptămâni până la
obţinerea rezultatului;
• în măsura posibilităţilor se vor implementa testele
de diagnostic rapid, în special în cazul suspiciunii de MDR-TB si XDR-TB.
De la o persoană suspectă de TB
pulmonară sau laringiană trebuie să fie examinate cel puţin 3 eşantioane de
spută prin microscopie şi cultură.
Confirmarea diagnosticului de TB pulmonară şi
instituirea tratamentului se fac de către medicul specialist pneumoftiziolog.
Testarea
sensibilităţii
PNCT are în vedere nu numai identificarea şi tratarea
bolnavilor sursă de infecţie, dar şi limitarea apariţiei şi răspândirii
tulpinilor cu rezistenţă la medicamentele antituberculoase. Rezistenţa
tulpinilor este în general consecinţa tratamentului incorect prescris sau
incorect administrat, putând duce la eşec terapeutic. Spectrul de
sensibilitate/rezistenţă a tulpinilor micobacteriene poate fi determinat cu
ajutorul antibiogramei.
Rezistenţa primară (iniţială)
a tulpinilor de MT se întâlneşte la pacienţii care nu au primit niciodată vreun
tratament antituberculos şi care s-au infectat cu bacili chimiorezistenţi.
Rezistenţa dobândită (secundară)
a tulpinilor de MT poate fi întâlnită la pacienţii care au primit cel puţin o
lună tratament antituberculos. Poate fi afirmată doar în situaţia în care avem
dovada sensibilităţii iniţiale a tulpinii (înainte de începerea tratamentului
antituberculos).
Rezistenţa globală reprezintă
prevalenta rezistenţei tulpinilor tuturor cazurilor de TB, indiferent dacă au
avut sau nu tratament antituberculos anterior, într-un an şi o ţară dată.
Principiul antibiogramei: indiferent de metoda de testare folosită, se compară creşterea
bacteriană de pe tuburile-test (conţinând medicamente) cu cea de pe
tuburile-martor, după însămânţarea unui eşantion reprezentativ din populaţia
bacilară de testat. In măsura posibilităţilor se vor implementa metodele de
testare rapidă, în special în cazul suspiciunii de MDR-TB şi XDR-TB.
Diagnosticul radiologie: modificările radiologice din TB pulmonară (leziunile infiltrative,
cavitare, fibrotice) au sensibilitate mare, dar specificitate redusă; nu sunt
patognomonice pentru TB. Diagnosticul pozitiv de TB nu se pune pe baza
examenului radiologie, ci doar pe baza celui bacteriologic.
Modificările radiologice sunt utilizate ca argumente
pentru diagnosticul TB pulmonare neconfirmate bacteriologic.
Testul cutanat la tuberculina este utilizat ca metodă convenţională curentă pentru depistarea
infecţiei cu MT. Singurul test acceptat în scop diagnostic şi epidemiologie
dintre cele folosite este IDR Mantoux.
Testul tuberculinic este utilizat:
• în scop diagnostic, pentru evidenţierea
sensibilizării la tuberculina în cazul unei suspiciuni de infecţie TB la copiii
simptomatici sau la cei din focare de TB (simptomatici
ori nu) cu ocazia AE;
• ca metodă de investigaţie epidemiologică, pentru
calculul prevalentei infecţiei şi al RAI, ca indicatori ai endemiei de TB;
• pentru toţi copiii simptomatici suspecţi de TB;
• pentru pacienţii cu infecţie HIV;
• pentru copii, la intrarea în centre de plasament,
şcoli ajutătoare, şcoli de corecţie şi alte instituţii cu risc;
• pentru aprecierea eficienţei vaccinării BCG.
Până în prezent produsul biologic utilizat în România
pentru intradermoreacţie este PPD, care la noi în ţară este fabricat de
Institutul Naţional de Cercetare-Dezvoltare pentru Microbiologie şi Imunologie
„Cantacuzino" Bucureşti - condiţionat în fiole de 2 ml şi poate avea două
concentraţii diferite: 2 UI/0,1 ml sau 10 UI/0,1 ml; fiecare fiolă de 2 ml
conţine aşadar 20 de doze. Fiolele care conţin 2 UI/0,1 ml sunt marcate cu
roşu, iar cele care conţin 10 UI/0,1 ml sunt marcate cu albastru. Pe fiole este
marcată data-limită a valabilităţii. Fiolele se păstrează la frigider, produsul
fiind sensibil la lumină şi căldură.
Reacţia (intens) pozitivă la PPD este marker al
infecţiei TB, nu certifică TB activă.
Pentru detalii legate de tehnica testării la
tuberculina şi interpretarea rezultatelor a se vedea anexa nr. 6, care face
parte integrantă din prezentele norme metodologice.
B. Diagnosticul TB extrapulmonare
Este în responsabilitatea medicului specialist de organ
afectat de TB, fiind susţinut în special de examenul histopatologic.
Diagnosticul TB extrapulmonare este dificil şi se face
prin excluderea altor condiţii patologice de către medicii din specialităţile
implicate. In cazul în care există localizări multiple, dintre care cel puţin
una este pulmonară, primează diagnosticul de TB pulmonară.
Cele mai frecvente localizări extrapulmonare ale TB
sunt: pleurezia TB, limfadenita TB, TB osteo-articulară, TB urogenitală,
pericardita TB, TB peritoneală şi ascita TB, TB gastro-intestinală, laringita
TB, TB oculară, TB otică, TB endocrină, TB cutanată, meningita TB (cu sau fără
TB miliară).
TB miliară este o formă deosebit de gravă, diseminată. Poate afecta pulmonul,
meningele şi/sau alte organe (ficat, splină, retină). Semne şi simptome: febră,
frisoane, anorexie, pierdere în greutate, astenie fizică, semne respiratorii
şi/sau meningeale. Forma acută este rapid progresivă.
Radiografia toracică (în cazul localizării pulmonare)
arată un aspect micronodular difuz, distribuit uniform. Pot exista
hepatomegalie şi, mai rar, splenomegalie. Examenul fundului de ochi poate arăta
tuberculi coroidieni.
Diagnostic: examenul
bacteriologic pentru BAAR este rar pozitiv în spută. Intrucât leziunile TB sunt
generalizate, produsele patologice recoltate din plămân, ficat, splină, măduvă
etc. pot oferi confirmarea diagnosticului.
Este recomandat ca ori de câte ori este posibil să se efectueze examen bacteriologic pentru evidenţierea
micobacteriilor.
C. Diagnosticul TB la copil
Diagnosticul TB la copil este foarte dificil. Pentru
diagnosticul pozitiv sunt luate în considerare următoarele criterii:
1. contactul cu un bolnav de TB eliminator de bacili;
2. IDR la PPD pozitiv la:
• copil nevaccinat BCG cu viraj tuberculinic recent;
• copil vaccinat BCG (cicatricea vaccinală > 3 mm)
cu salt tuberculinic (> 10 mm între două testări succesive);
3. context clinic sugestiv: tuse persistentă de peste 3 săptămâni, deficit ponderal de peste
10%, subfebrilitate şi dispnee fără altă cauză, kerato-conjunctivită
flictenulară, eritem nodos;
4. aspect radiologie sugestiv: adenopatii hilare sau
mediastinale, condensări de tip pneumonie sau bronhopneumonic cu
hipertransparenţe incluse, cu/fără reacţii pleurale ori atelectazii;
5. examen bronhoscopic: fistule, compresiuni sau
stenoze bronşice, ţesut de granulaţie perifistular;
6. examen bacteriologic pozitiv în aspiratul gastric
matinal sau bronşic.
PREVENIREA ÎMBOLNĂVIRILOR DE TB, MASURI DE LIMITARE
A EXTINDERII FOCARULUI DE TB
Focarul de TB reprezintă
un cumul de minimum 3 cazuri înregistrate între care există legătură
epidemiologică.
Măsuri aplicate în focarul de TB
Metodologia AE se referă la
folosirea anamnezei pentru identificarea contacţilorşi la utilizarea unor
investigaţii specifice şi nespecifice (IDR la PPD, examen radiologie, examen
bacteriologic) ale căror indicaţii şi interpretare sunt de competenţa medicului
pneumoftiziolog.
DPF declanşează AE în maximum 48 de ore de la primirea
Fişei de anunţare a cazului de TB.
AE este declanşată de medicul pneumolog din DPF în a
cărui arie teritorială a apărut cazul/focarul, cu informarea epidemiologului de
la nivelul ASPJ cu responsabilităţi în derularea PNCT
Atribuţii în efectuarea AE
Medicul pneumolog din DPF:
- iniţiază AE, organizează şi participă direct la
aplicarea măsurilor profilactice şi antiepidemice în focar;
- efectuează (împreună cu medicul de cabinet medical de
familie/şcolar/de medicină generală de întreprindere/medicina muncii) AE în
cazurile suspecte sau confirmate de TB, asigurând controlul contacţilor
(control clinic, biologic, bacteriologic, radiologie etc);
- răspunde de calitatea AE (atât la adulţi, cât şi la
copii) şi de finalizarea acestora;
- raportează focarele cu mai mult de 3 cazuri din
colectivităţi şcolare/de muncă la ASPJ - Compartimentul epidemiologie.
Date minimale raportate:
- data debutului;
- numărul de cazuri;
- localizarea evenimentului: tip colectivitate/efectiv (număr de persoane expuse la risc);
- statusul curent al cazurilor;
- măsurile întreprinse.
MF, medicul din cabinetul şcolar sau cel care asigură
servicii de medicina muncii:
1. participă efectiv la AE de filiaţiune prin
identificarea tuturor contacţilor şi trimiterea lor la control de specialitate;
2. aplică măsurile indicate de medicul pneumolog din
DPF teritorial (tratament ambulatoriu sub directă supraveghere,
chimioprofilaxie);
3. efectuează educaţia pentru sănătate a bolnavilor de
TB şi familiilor acestora;
4. identifică suspecţii cu fenomene respiratorii si îi
îndrumă la DPF.
Rolul medicului epidemiolog în cadrul AE:
- informează ierarhic institutul de sănătate publică
regional, Centrul pentru prevenirea şi controlul bolilor transmisibile din
Institutul de Sănătate Publică Bucureşti şi ASP-MSP asupra apariţiei şi
evoluţiei focarului, conform legislaţiei în vigoare;
- participă împreună cu medicul pneumolog coordonator
la efectuarea AE în focarele cu cazuri multiple din colectivităţi de
copii/adulţi;
- analizează rezultatele investigaţiilor descriptive
obţinute de medicul pneumolog CTJ împreună cu medicul de cabinet (MF, medicul
din cabinetul şcolar şi medicul care asigură servicii de medicina muncii) din
focarul de colectivitate;
- evaluează acţiunile derulate
în cadrul AE: depistare activă, măsuri faţă de bolnavi, contacţi, suspecţi,
dezinfecţie şi eficienţa acestora;
- estimează nivelul de afectare al colectivităţii (loc
de muncă sau şcoală);
- elaborează împreună cu medicul pneumolog CTJ şi
medicul din DPF strategia de control al focarului în vederea limitării
răspândirii infecţiei;
- evaluează eficienţa măsurilor recomandate, situaţia
epidemiologică şi propune, dacă este nevoie, măsuri suplimentare de supraveghere/control
al focarului.
MANAGEMENTUL CAZURILOR DE TB
Cazul de TB este:
• bolnavul cu TB confirmată bacteriologic ori
histopatologic (HP); sau
• bolnavul care nu are confirmare, dar la care medicul
pneumolog decide începerea tratamentului antituberculos.
Orice instituire a tratamentului
antituberculos trebuie avizată de către medicul pneumolog din teritoriul în
care se află unitatea sanitară respectivă, pentru asigurarea anunţării şi
înregistrării cazului respectiv de TB.
Inregistrarea şi declararea
După depistarea/primirea fişei de anunţare a unui caz
de TB (chiar decedat), dacă pacientul locuieşte la adresa comunicată, DPF
anunţă în termen de 3 zile apariţia cazului - prin scrisori medicale - MF şi
medicului epidemiolog/de sănătate publică al teritoriului, pentru declanşarea AE.
Totodată, pacientul este înregistrat atât în Registrul
de TB, cât şi în baza de date electronică din calculatorul unităţii.
Cazul de TB este definit în funcţie de localizarea
bolii: pulmonară sau extrapulmonară, istoricul terapeutic (sistem OMS) sau
confirmarea bacteriologică ori histopatologică (sistem ECDC) (anexa nr. 8, care
face parte integrantă din prezentele norme metodologice).
In cadrul acestui program vor fi utilizate ambele
tipuri de definiţii.
In funcţie de istoricul terapeutic, un caz de TB poate fi:
1. Caz nou (N) -
pacientul care nu a luat niciodată tratament cu medicamente antituberculoase în
asociere pe o perioadă mai mare de o lună de zile.
La încadrarea pacientului „Caz nou" nu se ia în
considerare chimioterapia preventivă, efectuată cu un singur medicament (sau cu
două, ca de exemplu în cazul persoanelor infectate cu HIV);
2. Caz cu retratament -
unul dintre următoarele categorii:
• Recidivă (R) - pacientul care a fost evaluat „Vindecat" sau „Tratament complet"
în urma unui tratament antituberculos anterior şi care
are un nou episod de TB confirmat bacteriologic sau HP. Cazurile de TB
neconfirmate pot fi înregistrate ca „Recidivă" în baza deciziei
colectivului medical;
• Retratament pentru eşec
(E) - pacientul care începe un retratament după ce a fost evaluat ca „Eşec" al unui tratament
anterior;
• Retratament pentru abandon (A) - pacientul care începe un retratament după ce a fost evaluat ca
„Abandon" al unui tratament anterior şi este bacteriologic pozitiv sau la
care medicul pneumolog decide reluarea unui nou tratament după abandonul celui
anterior;
• Cronic (C) - pacientul
care începe un nou retratament după ce a fost evaluat ca „Eşec" al unui
retratament anterior.
Odată cu intrarea în funcţiune a ECDC, pentru
integrarea TB printre celelalte boli transmisibile, cazurile de TB vor fi
clasificate şi din punct de vedere epidemiologie în certe, probabile şi
posibile.
Numărul de cazuri conform definiţiilor de caz
recomandate de ECDC vor putea fi extrase automat prin prelucrarea datelor din
baza naţională din Fox-Pro. Aceste definiţii se regăsesc în anexa nr. 8.
Anunţarea
Pentru orice caz de TB la care se decide începerea
tratamentului antituberculos, se va completa fişa de anunţare în cel mult 48 de
ore. Fişa de anunţare este completată de către medicul care a diagnosticat
cazul sau care a iniţiat tratamentul şi este imediat trimisă (prin fax sau prin
poştă) DPF de pe teritoriul căruia locuieşte în fapt bolnavul, indiferent de
adresa înscrisă în documentele sale de identitate.
După înregistrare, cazul este raportat în baza
naţională de date prin conectare prin internet la serverul din UCM a PNCT.
Fişa de anunţare a cazului de MDR-TB este completată
ori de câte ori este diagnosticat un caz de MDR-TB şi este trimisă centrului de
excelenţă MDR-TB arondat, CTJ al PNCT, precum şi Unităţii centrale de
supraveghere a tuberculozei de la INPMN. Instituirea tratamentului pentru
această categorie de bolnavi se va face numai cu avizul comisiei din centrul
MDR-TB de la Bucureşti sau Bisericani.
Fişa de declarare - generată de aplicaţia software - se
imprimă, se semnează şi se parafează. Toate fişele generate în cursul unei luni
sunt transmise la ASPJ în primele 5 zile ale lunii următoare. De la ASPJ sunt
trimise la UCM a PNCT până cel târziu la data de 10 a lunii următoare celei de
raportare.
Dacă pacientul nu locuieşte la adresa indicată, se vor
face toate demersurile pentru a afla adresa reală. Dacă aceasta nu poate fi
identificată, cazul va fi totuşi înregistrat de către DPF pe raza căruia se
află cea mai probabilă adresă şi, dacă pacientul nu se prezintă timp de două
luni de la externare, va fi evaluat ca „Pierdut".
Infirmarea
Dacă după înregistrare se constată că diagnosticul de
TB activă nu a fost corect, cazul respectiv este infirmat de către medicul
pneumolog din DPF care a înregistrat cazul. Când infirmarea este făcută de
către o altă unitate, aceasta este comunicată DPF prin Fisa de anunţare a
infirmării diagnosticului de TB.
Decesul
In cazul decesului unui bolnav de TB în spital, în
termen de 48 de ore se completează Fişa de anunţare a
decesului în spital, care se trimite DPF. In cazul în care diagnosticul de TB
este pus cu ocazia necropsiei, se completează Fişa de anunţare a cazului de TB,
în vederea efectuării AE şi declarării post-mortem a cazului de către DPF.
Transferul
Dacă un caz îşi schimbă adresa după înregistrare până
la momentul evaluării, se va opera electronic în aplicaţie transferul, iar după
primirea confirmării preluării pacientului, se va evalua ca „Mutat" de
către primul DPF şi se va trimite documentaţia medicală celui de-al doilea DPF.
Dacă pacientul nu apare la noua adresă în maximum două
luni de la operarea transferului, primul DPF va evalua cazul ca „Pierdut"
(P).
Pentru detalii privind anunţarea, înregistrarea şi
declararea cazurilor se va consulta anexa nr. 9, care face parte integrantă din
prezentele norme metodologice.
Cazurile de MDR-TB vor
fi încadrate în plus şi conform categoriilor speciale, în funcţie de istoricul
terapeutic, după cum urmează:
- atât într-o categorie de caz
de TB, conform definiţiilor cazurilor la înregistrare;
- cât şi în una dintre categoriile următoare, conform
anamnezei terapeutice:
1. caz nou de MDR-TB - pacientul care nu a primit
înainte de episodul actual tratament antituberculos în asociere mai mult de o lună;
2. caz de MDR-TB tratat anterior numai cu medicamente
de linia I - pacientul care a primit anterior
episodului actual tratament antituberculos mai mult de o lună, dar numai cu
medicamente de linia I;
3. caz de MDR-TB tratat anterior cu medicamente de
linia a II-a - pacientul care a primit în
antecedente tratament antituberculos mai mult de o lună cu medicamente de linia
a II-a, indiferent dacă împreună cu sau fără medicamente de linia I.
Pe parcursul tratamentului pacienţii cu MDR-TB vor fi
evaluaţi din 12 în 12 luni (în categoria „Continuă tratamentul"), dar
evaluarea finală se va face la 3 ani de la instituirea tratamentului pentru
MDR-TB sau în orice moment înainte de împlinirea celor 3 ani, dacă intervine o
situaţie ireversibilă (abandon, eşec al tratamentului, pacient pierdut, deces).
In intervalul acestor 3 ani se face evaluarea
intermediară (monitorizare periodică) privind evoluţia bacteriologică.
Conversia culturii se
înregistrează în momentul în care pacientul cu o cultură iniţial pozitivă, după
începerea tratamentului pentru MDR-TB, are două rezultate succesive ale
culturii (efectuate la interval de minimum 30 de zile) negative.
Cazurile de MDR-TB sunt anunţate, declarate şi
înregistrate atât în Registrul de TB, cât şi în aplicaţia pentru gestionarea datelor de endemie de TB.
In momentul confirmării diagnosticului de MDR-TB şi al
înregistrării cazului, în aplicaţie se deschide un câmp special pentru MDR-TB,
unde se vor înscrie datele de înregistrare, monitorizare şi evaluare.
Cazurile de MDR-TB pot fi
introduse în aplicaţie atât de la DPF, cât şi de la cele două centre de
excelenţă pentru MDR-TB de la Bucureşti şi Bisericani.
TRATAMENTUL TB
Scop:
- vindecarea pacienţilor;
- reducerea riscului de recidive;
- prevenirea deceselor;
- prevenirea instalării
chimiorezistenţei la MT;
- prevenirea complicaţiilor şi limitarea răspândirii
infecţiei.
Principii care se impun pentru creşterea eficienţei
terapiei şi prevenirea
instalării chimiorezistenţei:
- terapie standardizată;
- terapie etapizată (regimuri
bifazice):
• faza de atac (iniţială sau intensivă);
• faza de continuare;
- asocierea medicamentelor anti TB;
- regularitatea şi continuitatea administrării,
asigurându-se întreaga cantitate de medicamente necesară pentru întreaga durată
a tratamentului;
- individualizarea terapiei numai în următoarele
situaţii:
• chimiorezistenţa la MT;
• alte micobacterii;
• reacţii adverse majore;
• boli asociate şi interacţiuni medicamentoase;
- gratuitatea tuturor mijloacelor terapeutice necesare,
inclusiv medicaţia de suport, pentru toţi bolnavii de
TB;
- se recomanda administrarea tratamentului sub directa
observaţie, pe toata durata acestuia.
Clasificarea medicamentelor antituberculoase:
- medicamente antituberculoase de primă linie
(esenţiale);
- medicamente de rezervă
(linia a II-a) - prezentate la cap. „Tratamentul TB multidrog rezistente
MDR/XDR-TB".
Din categoria medicamentelor anti TB de primă linie fac
parte: Izoniazida, Rifampicina, Pirazinamida, Streptomicina şi Etambutolul.
Aceste medicamente au următoarele proprietăţi importante: acţiune bactericidă;
capacitate de sterilizare; capacitate de a preveni instalarea
chimiorezistenţei.
Tabelul 1: Medicamente
anti TB esenţiale, mod de acţiune, forme de
prezentare, cale de administrare, dozaj în funcţie
de ritmul de administrare
|
Medicamentul
|
Forma de prezentare
|
Modul de acţiune
|
Calea de administrare
|
Ritmul de administrare
|
|
7/7 (mg/kg)
|
3/7 (mg/kg)
|
|
Izoniazida (H)
|
tb. de 100 mg şi 300 mg; sol. apoasă (100 mg/ml)
|
bactericid
|
oral/i. m.
|
5-10
|
10-15
|
|
Rifampicina (R)
|
cps.de 150, 300 mg
|
bactericid
|
oral
|
10
|
10
|
|
Etambutol (E)
|
tb. de 400 mg, cps. de 250 mg
|
bacteriostatic
|
oral
|
15-25
|
30-50
|
|
Streptomicina (S)
|
sol. apoasă, fiole de 1 g
|
bactericid
|
i.m., i.v.
|
20
|
20
|
|
Pirazinamida (Z)
|
tb. de 500 mg
|
bactericid
|
oral
|
20-30
|
35-40
|
Combinaţiile în doze fixe de medicamente
antituberculoase întrucât asigură creşterea compliantei şi previn
monoterapia includ cel puţin Izoniazida şi Rifampicina. Sunt recomandate
accidentală care ar putea produce chimiorezistenţa.
Tabelul 2: Dozele maxime admise la medicamentele anti
TB
|
Medicamentul
|
Doza
|
|
7/7
|
3/7
|
|
Izoniazida
|
300 mg
|
900 mg
|
|
Rifampicina
|
600 mg
|
600 mg
|
|
Pirazinamida
|
2.000 mg
|
3.000 mg
|
|
Etambutol
|
1.600 mg
|
2.000 mg
|
|
Streptomicina
|
1g
|
1g
|
Regimuri terapeutice
Regimurile de chimioterapie folosite pentru
tratamentul TB sunt standardizate şi de scurtă durată.
Pentru fiecare pacient care începe un tratament
antituberculos se completează Fişa de tratament al tuberculozei (anexa nr. 10,
care face parte integrantă din prezentele norme metodologice).
Pentru a facilita comunicarea pe plan internaţional au
fost stabilite coduri/simboluri care permit identificarea regimurilor
terapeutice, asocierea de medicamente recomandate etc.
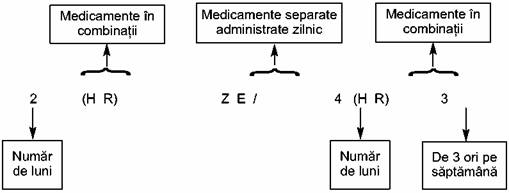
Un regim terapeutic are două faze: o fază
iniţială/intensivă şi una de continuare. Cifra plasată înaintea fazei
reprezintă durata acesteia în luni. Literele înscrise în paranteze
reprezintă medicamentele
combinate în doze fixe utilizate. Numărul ce apare subscris după literele din
paranteză indică numărul de doze pe săptămână. Dacă acest număr nu există,
înseamnă că tratamentul se administrează zilnic (sau 6 din 7 zile, excluzând
duminica).
Exemplu: 2(HR)ZE/4(HR)3:
- faza iniţială durează două luni; în această fază se
administrează zilnic Izoniazida şi Rifampicina în formă combinată şi doză fixă,
asociate cu Pirazinamida şi Etambutol în forme de prezentare şi administrare
separată;
- faza de continuare durează 4 luni; în această fază se
continuă administrarea Izoniazidei şi Rifampicinei în formă combinată şi doză
fixă, cu un ritm de administrare de 3 ori/săptămână.
Figura 1: Simboluri folosite în schema de tratament
Tabelul 3: Categorii
de tratament în funcţie de forma de boală
|
Regimul
|
Forma de TB
|
Asociere de medicamente
|
|
Faza de atac 7/7
|
Faza de continuare 3/7
|
|
I
|
• Pulmonară, caz nou
• Extrapulmonara, caz nou
|
2 HRZE*) sau
2 HRZS*)
Observaţie: la cazurile cu frotiu pozitiv
la T2: 3 HRZE(S)
|
4HR
3HR
Observaţie: la cazurile extrapulmonare severe, faza de continuare
se prelungeşte la 6-10 luni
|
|
II
|
Pulmonară M+ la prim retratament:
• recidive la cazuri la care nu s-a confirmat o chimiorezistenţă
• eşec al tratamentului iniţial
• tratament după abandon
|
2 HRZSE + 1 HRZE Observaţie: sunt necesare antibiograme fiabile
preterapeutic şi la cazurile încă pozitive la T3
|
5HRE
|
|
Individualizat
|
Cazuri de MDR-TB sau de reacţii adverse severe
|
Pentru această categorie sunt recomandate regimuri
individualizate.
|
*) La copii (0-14 ani) se poate renunţa la
administrarea Etambutolului sau a Streptomicinei.
Administrarea tratamentului se face iniţial în spital,
ulterior în ambulatoriu, sub directa observare până la încheierea acestuia.
Spitalizarea cazurilor de TB pulmonară cu microscopie negativă şi
extrapulmonara trebuie să fie limitată numai la cazurile severe; există
posibilitatea reducerii duratei de spitalizare chiar la cazurile pulmonare cu
microscopie pozitivă, dacă tratamentul direct observat poate fi administrat în
ambulatoriu.
Tratamentul TB latente se referă la persoanele
cunoscute a fi infectate cu MT, dar care nu sunt bolnave de TB. Acesta nu este
recomandat de rutină, având în vedere problemele ridicate: necesitatea
excluderii TB ca boală, necesitatea asigurării compliantei la tratament,
numărul mare de persoane infectate, costurile şi personalul necesar, evidenţa
acestor cazuri etc.
Tabelul 4: Indicaţiile
tratamentului TB latente
|
Factorul de risc
|
Rezultatul reacţiei cutanate la PPD
|
|
Contacţi în vârsta de până la 15 ani ai pacienţilor cu TB
pulmonară cu microscopie pozitivă
|
>= 10 mm
|
|
Infecţia HIV
|
>= 5 mm
|
|
Bolnavi cu afecţiuni cronice cu risc important de imunodepresie
(urmează terapie biologică sau cu alte medicamente imunodeprimante) şi/sau
care vin în contact cu bolnavi cu TB pulmonară cu microscopie pozitivă
|
>= 10 mm
|
Inainte ca aceşti pacienţi să fie trataţi, se va
efectua o anamneză atentă, un examen clinic şi radiografie pentru excluderea
unei TB active şi pentru obţinerea de informaţii asupra chimiosusceptibilităţii
MT a sursei de infecţie.
Regimul standard folosit: cu H, 5 mg/kgc (maximum 300 mg), 10 mg/kgc la copii, în administrare zilnică, timp
de 6 luni (9-12 luni la HIV+).
Monitorizarea tratamentului preventiv se face prin
examen clinic; controlul lunar al funcţiei hepatice şi renale se recomandă în
cazul în care se suspicionează efecte secundare sau la pacienţii care au
afecţiuni hepatice ori renale cronice; se va întrerupe administrarea
medicamentelor dacă AST sau ALT au valori de 5 ori mai mari decât normalul ori dacă pacienţii sunt
simptomatici (anorexie, greţuri, vărsături, ficat
sensibil la palpare).
Pentru a spori complianţa la tratament se va discuta cu
pacientul, cu părinţii, se va aplica DOT, se vor acorda stimulente.
Monitorizarea tratamentului
Monitorizarea evoluţiei este:
- clinică: creştere în greutate, afebrilitate,
dispariţia tusei;
- radiologică: reducerea cavităţilor, ştergerea
infiltratelor, fibrozarea nodulilor;
- bacteriologică.
Tabelul 5: Periodicitatea
monitorizării evoluţiei sub tratament prin controlul sputei (microscopie şi
cultură)
|
Momentul controlului
|
Categoria I
|
Categoria II
|
Individualizat*)
|
|
La momentul diagnosticului (3 produse)
|
T0
|
T0
|
T0
|
|
La sfârşitul fazei iniţiale (două produse)
|
T2**)
|
T3**)
|
T2
|
|
In faza de continuare (două produse)
|
T4
|
T5
|
|
|
La sfârşitul tratamentului (două produse)
|
T6
|
T8
|
|
*) Se recomandă efectuarea
lunară sau la două luni a examenului microscopic şi a culturilor pentru
pacienţii multidrog rezistenţi; antibiograma nu se va repeta decât după 6 luni
de menţinere a pozitivităţii sau la indicaţii speciale.
**) In cazul pozitivităţii se repetă după o lună, timp
în care se continuă faza intensivă.
Examenul clinic şi radiologic au numai un rol
orientativ în monitorizarea evoluţiei sub tratament.
Reacţiile adverse şi interacţiunea cu alte
medicamente
Acestea sunt detaliate în anexa nr. 11, care face parte integrantă din prezentele norme metodologice.
TRATAMENTUL TB ÎN SITUAŢII SPECIALE
1. TB la persoane infectate cu HIV
Principii:
Tratamentul va fi instituit în colaborare cu medicul
infecţionist care tratează pacientul cu HIV.
Se administrează schemele
terapeutice standard.
Răspunsul terapeutic cel mai bun se obţine dacă schema
terapeutică include H şi R; R este indicată pe toată durata tratamentului; în
cazul în care se administrează antiretrovirale care interferează cu
Rifampicina, dacă este posibil, se amână iniţierea tratamentului
antiretroviral, dacă nu, se vor asocia cele două terapii, având în vedere
interacţiunea dintre R şi antiretrovirale; în faza de continuare se recomandă
asocierea HE până la 9 luni.
Rifabutina poate fi administrată
în doză de 10-20 mg/kgc/zi, în locul Rifampicinei, la pacienţii care primesc
terapie antiretrovirală.
2. TB la copil
Medicamentele anti TB esenţiale folosite în terapia
copilului sunt identice cu cele utilizate la adult.
Etambutolul nu este recomandat la vârste mici deoarece la această vârstă copilul nu sesizează
modificările funcţiei vizuale. Etambutolul în doze de 15 mg/kg/zi este bine
tolerat după vârsta de 5 ani. In comparaţie cu Streptomicina, care,
administrată injectabil, este dureroasă, Etambutolul are şi avantajul
administrării orale.
3. TB şi sarcina
Dacă femeile bolnave de TB sunt şi însărcinate, li se
administrează medicamentele anti TB esenţiale (HRZE), exceptând Streptomicina,
care este ototoxică pentru făt şi este interzisă în timpul sarcinii. Gravida va
primi şi 10-20 mg Piridoxină/zi. Instituirea tratamentului antituberculos nu
reprezintă o indicaţie pentru avortul terapeutic.
Alăptarea este permisă, mama neîntrerupând tratamentul
anti TB.
Administrarea chimioterapiei preventive va fi luată în
considerare în funcţie de statusul bacteriologic al mamei şi de momentul
instituirii tratamentului antituberculos al acesteia. In cazul în care mama are
examen bacteriologic pozitiv la examinarea microscopică a sputei în momentul
naşterii sau chiar dacă este negativată, dar nu a încheiat tratamentul
antituberculos, se poate lua în considerare administrarea chimioterapiei
preventive cu Izoniazidă la noul-născut, cu atenta monitorizare a funcţiei
hepatice a acestuia şi asocierea de Piridoxină.
Vaccinarea BCG va fi amânată
până la terminarea chimioterapiei preventive şi numai după testarea la
tuberculină a sugarului.
4. Contracepţia
orală în TB
Rifampicina interacţionează cu medicaţia contraceptivă
orală scăzând nivelul de protecţie a anticoncepţionalelor.
O bolnavă de TB activă sexual trebuie sfătuită să
utilizeze două mijloace contraceptive, dintre care unul mecanic.
5. TB şi bolile
hepatice
H, R şi Z au efecte hepatotoxice. Dintre acestea Z are
cea mai mare activitate hepatotoxică. Din acest motiv la bolnavii cu afecţiuni
hepatice cu citoliză se recomandă evitarea administrării Z.
Dacă în timpul administrării tratamentului apare
citoliză hepatică (cu valori ale transaminazelor de cel puţin 5 ori mai mari),
se întrerupe tratamentul până la normalizarea probelor hepatice (7-10 zile) şi se reia cu doze scăzute 2-3 zile şi apoi cu
doza întreagă.
Terapia anti TB la bolnavul hepatic include HR şi alte
două chimioterapice fără hepatotoxicitate (de exemplu: S şi E). In această
situaţie se va prelungi tratamentul până la 9-12 luni.
Nu există consens terapeutic pentru hepatita virală
acută. Unii autori recomandă întreruperea tratamentului anti TB până la
vindecarea hepatitei, alţii recomandă pentru faza iniţială 2 HSE şi pentru faza de continuare 6-9
HE.
In cazul constatării creşterii
transaminazelor hepatice la valori de 5 ori mai mari decât cele normale, se va
întrerupe tratamentul anti TB până la normalizarea rezultatului probelor
biologice, după care se reia tratamentul antituberculos. Atitudinea va fi
individualizată în funcţie de fiecare pacient.
6. TB la bolnavul cu
insuficienţă renală
H, R şi Z se administrează în doze normale.
S şi E se elimină pe cale renală, motiv pentru care se
vor folosi doze mici (în funcţie de clearance-ul la creatinina) şi se va
monitoriza funcţia renală pe durata tratamentului cu aceste medicamente.
Acestor pacienţi li se recomandă administrarea Z, E şi
S de 3 ori pe săptămână.
La bolnavii hemodializaţi, medicaţia anti TB se
administrează imediat după şedinţa de hemodializă.
TRATAMENTUL UNOR
FORME SPECIALE DE TB EXTRAPULMONARĂ
In TB extrapulmonară, abordarea terapeutică este
multidisciplinară.
1. Meningita TB
Etambutolul şi Streptomicina au o penetrabilitate
redusă la nivelul meningelui. Penetrabilitatea acestora este ameliorată în
condiţiile meningelui inflamat. Din aceste motive aceste medicamente se vor
utiliza doar în situaţii de necesitate şi în special în faza iniţială. H: 15
mg/kg/zi, Z: 40 mg/kg/zi, R: 20 mg/kg/zi, S: 40 mg/kg/zi, E: 20 mg/kg/zi.
Pentru obţinerea unor concentraţii eficiente în
lichidul cefalorahidian (LCR) şi în ţesuturile intracraniene se recomandă
folosirea unor doze mai mari:
- în faza iniţială, pe o perioadă de două luni, se
recomandă 4 antituberculoase: H, R, Z, S sau E. In faza de continuare se
recomandă timp de 4-10 luni două antituberculoase: H, R;
- corticoizii se recomandă, de rutină, sub formă de
Prednison, 2 mg/kg/zi (nedepăşind 60 mg/zi) pe o perioadă de 3-4 săptămâni,
după care se reduce progresiv doza, cu întreruperea tratamentului în 1-2
săptămâni.
2. Pericardita TB
Se recomandă terapie standardizată cu regim I; se asociază corticoterapia 1 mg/kg/zi,
timp de 4 săptămâni, cu scăderea progresivă a dozei în următoarele 7 săptămâni,
durata totală a corticoterapiei fiind de 11 săptămâni.
3. TB osteoarticulară
Tratament cu fază intensivă cuprinzând 4 medicamente
antituberculoase (H, R, Z, E) timp de două luni şi tratament de continuare cu
H, R în următoarele 7 luni
Uneori este necesar tratamentul chirurgical sau
ortopedic.
4. TB ganglionară
Având în vedere caracteristica
MP a leziunilor din TB ganglionară, respectiv penetraţia dificilă a
antituberculoaselor la nivelul maselor cazeoase, tratamentul se poate prelungi
până la 9 luni.
5. Empiemul TB
Necesită asocierea tratamentului medicamentos
antituberculos cu cel chirurgical.
TB cu germeni rezistenţi la medicamentele
antituberculoase
Pentru identificarea spectrului de sensibilitate al
tulpinilor de MT izolate este esenţială efectuarea corectă a testelor de sensibilitate la medicamentele antituberculoase. Suspiciunea de rezistenţă la medicamentele antituberculoase poate fi
clinică, dar certitudinea
este dată de rezultatul testului de sensibilitate in
vitro (antibiograma).
Tabelul 6: Tipuri de
chimiorezistenţe în funcţie de rezistenţele identificate la testele de sensibilitate in vitro
|
Tip de chimiorezistenţă
|
Rezistenţă la
|
|
Monorezistenţa
|
o singură substanţă
|
|
Polirezistenţa
|
două sau mai multe substanţe (excluzând combinaţia H+R)
|
|
MDR-TB
|
H+R cu sau fără rezistenţă la alte substanţe
|
|
XDR-TB
|
H+R asociată cu rezistenţă la o Quinolonă şi un drog injectabil
de linia a II-a
|
In funcţie de istoricul terapeutic al pacientului, se
definesc următoarele tipuri de chimiorezistenţe:
- Chimiorezistenţă primară (iniţială) este chimiorezistenţă identificată la pacienţii
netrataţi anterior. In acest caz este vorba de o sursă de infecţie cu bacili
rezistenţi.
- Chimiorezistenţă secundară
(chimiorezistenţă identificată la pacienţii
trataţi anterior) este definită ca rezistenţa care apare prin selecţia de
mutanţi chimiorezistenţi, în urma unui tratament (tratamentul anterior este
definit ca tratamentul pentru TB activă mai mult de o lună).
In cazul monorezistenţei la H sau R, se recomandă prelungirea
tratamentului antituberculos până la 12 luni în cazul rezistenţei la H şi 18
luni în cazul rezistenţei la R.
Tratamentul TB multidrogrezistente MDR/XDR-TB
Tratamentul TB multidrogrezistente are importanţă
practică deosebită datorită costurilor mari pe care le implică şi
dificultăţilor provocate de durata prelungită, cu medicamente greu de tolerat.
In aplicarea PNCT se vor respecta recomandările din
„Ghidul pentru managementul cazurilor de tuberculoză multidrog rezistentă (TB
MDR)", ediţia 2005, care cuprinde principiile generale de diagnostic şi
îngrijire a cazurilor de TB produsă cu germeni rezistenţi la medicamentele
antituberculoase esenţiale.
Pentru a se evita erorile generate de utilizarea
neraţională a medicamentelor de linia a II-a, orice tratament cu aceste
medicamente nu va putea fi început decât după discutarea în cadrul comisiilor
care funcţionează în centrele de excelenţă de la Bucureşti şi Bisericani, care
vor indica regimul de tratament pentru fiecare caz în parte.
Se recomandă internarea tuturor pacienţilor în unităţi
spitaliceşti care vor fi autorizate să efectueze tratament cu medicamente de
linia a II-a. Centrele specializate de tratament al TB chimiorezistenţe (de la
Bucureşti, din cadrul INPMN, şi de la Bisericani, judeţul Neamţ) trebuie
valorificate pentru tratamentul unui număr cât mai mare de pacienţi în faza
intensivă. Alte unităţi spitaliceşti care au primit sau vor primi autorizarea
să efectueze tratament cu medicamente de linia a II-a trebuie să aibă
posibilitatea să efectueze investigaţiile bacteriologice necesare monitorizării
într-un laborator cu control al calităţii asigurat. De asemenea, unităţile
respective trebuie să aibă asigurate măsuri corespunzătoare de control al
transmiterii infecţiei tuberculoase. Pacienţii rămân spitalizaţi obligatoriu
cel puţin până la negativarea microscopică a sputei.
Pentru pacienţii la care
colectivul medical sau comisiile care funcţionează în centrele MDR-TB au
stabilit că nu au resurse terapeutice, se recomandă luarea tuturor măsurilor
necesare prin soluţii de izolare a cazurilor pentru limitarea transmiterii
infecţiei. La această categorie de pacienţi se va evita administrarea
medicamentelor antituberculoase, care nu au decât rolul de a induce fenomene
secundare şi cheltuieli nejustificate, fără a aduce niciun beneficiu
terapeutic.
Intrucât în tratamentul pacienţilor cu MDR/XDR-TB se
utilizează medicamente mai puţin active, mai greu de tolerat, mai scumpe şi cu
reacţii adverse mai frecvente, se impune respectarea anumitor reguli:
- administrarea medicamentelor trebuie să fie zilnică,
direct observată pe toată durata tratamentului;
- începerea tratamentului se poate face cu scheme
terapeutice empirice sau individualizate, în funcţie de spectrul de
sensibilitate al tulpinii izolate;
- tratamentul trebuie să cuprindă cel puţin 3
medicamente antituberculoase (preferabil 4 sau 5) la
care bacilii s-au dovedit a fi sensibili sau, în lipsa antibiogramei, minimum 3 medicamente care nu au fost încă administrate bolnavului şi care
nu prezintă rezistenţă încrucişată cu cele folosite anterior.
In cazul cunoaşterii sensibilităţii germenilor pentru
cazul sursă de infecţie, se recomandă începerea tratamentului în funcţie de
această informaţie.
Medicamentele cel mai greu tolerate pot fi împărţite în
cel mult două prize. Se preferă administrarea unei doze înainte de culcare
(numai pentru pacienţii internaţi în spital, sub directă observaţie).
Regimul de tratament individualizat utilizat pentru
tratamentul MDR-TB:
1. Are o fază iniţială empirică, până la finalizarea
antibiogramei la medicamentele de linia I şi a II-a de la T0, apoi schema se adaptează în funcţie de
rezultatele antibiogramei.
2. Stabilirea regimului de tratament se bazează pe
antibiograma efectuată pentru medicamentele de linia I
si a IIa (H/R/Z/E/S/K/PTM/CS/Q/PAS) într-un LNR.
3. In faza intensivă se folosesc 5-7 medicamente considerate a fi eficiente.
4. Schema va cuprinde un medicament injectabil
(S/Ak/K, Capreomicină).
5. Medicamentul injectabil se administrează zilnic
până la conversia culturii, apoi cel puţin încă 6 luni după conversia culturii,
de preferat tot zilnic.
6. In faza de continuare se
administrează pe cale orală 4
medicamente la care sensibilitatea este păstrată, pe toată durata
tratamentului.
7. Tratamentul se face în spital sau în centrul MDR-TB
până la conversia în cultură (minimum două culturi consecutive negative).
8. Durata optimă de spitalizare pentru MDR-TB este de
120 de zile, conform anexei 19 la Normele metodologice de aplicare a
Contractului-cadru privind condiţiile acordării asistenţei medicale în cadrul
sistemului de asigurări sociale de sănătate pentru anul 2008, aprobate prin
Ordinul ministrului sănătăţii publice şi al preşedintelui Casei Naţionale de
Asigurări de Sănătate nr. 522/236/2008.
9. Durata tratamentului este de 18 luni după conversia
culturii.
10. In ambulatoriu tratamentul se va continua obligatoriu sub directă observare.
11. Dozele folosite vor fi doze maximale.
Faza iniţiala, empirică (până la sosirea unei
antibiograme fiabile de la LNR)
Pacientul suspect de MDR-TB sau pacientul identificat
cu rezistenţă HR, până la obţinerea rezultatelor antibiogramei de linia a II-a,
va începe tratamentul după o schemă stabilită empiric, pe baza datelor privind
tratamentele anterioare sau pe baza spectrului de sensibilitate cunoscut al
sursei de îmbolnăvire. Stabilirea unui regim empiric, atât în spital, cât şi în
ambulatoriu, se poate face numai cu avizul colectivului medical al unităţii cu
paturi sau al celui de la nivel judeţean, ce se întruneşte periodic, şi/sau cu
avizul CTJ al PNCTsau al comisiei MDR-TB de la nivel judeţean.
Pentru fiecare pacient cu
MDR/XDR-TB care începe tratamentul se completează Fişa de tratament pentru
cazul cu MDR-TB şi Fişa de monitorizare a evoluţiei sub tratament a pacientului
cu MDR-TB (anexa nr. 12, care face parte integrantă din prezentele norme
metodologice).
In cazul în care se presupune
că germenii mai sunt sensibili la medicamente de linia I,
acestea se recomandă a fi folosite (E, Z,Ş).
In situaţia în care nu există certitudinea că este
vorba de MDR-TB, dar există o foarte mare probabilitate, se recomandă ca în
schemă să se utilizeze numai medicamente de linia I şi a II-a în afara H şi R, urmând ca în cazul identificării unei
sensibilităţi la R şi/sau H să se modifice schema.
La pacienţii care au avut eşecuri repetate după mai
multe reluări de tratament cu medicamente de linia I, sensibilitatea la aceste medicamente este puţin probabilă. In acest
caz se recomandă regimuri empirice care să cuprindă cel puţin 3 medicamente
neutilizate.
Pentru pacienţii cu multiple tratamente cu medicamente
de linia I şi a II-a, regimul
de tratament va conţine pe cât posibil medicamente care nu au fost disponibile
până în prezent în România (Capreomicina, PAS) şi medicamente ce nu au fost
folosite de către pacient.
Pentru pacienţii la care nu se pot întocmi scheme de
tratament cu cel puţin 3 medicamente active, se poate avea în vedere şi
asocierea Claritromicinei sau Amoxicilinei cu inhibitori de Beta-lactamază.
La pacienţii la care nu se poate întocmi o schemă
empirică cu cel puţin 3 medicamente neutilizate anterior, pe baza datelor de
anamneză terapeutică, pentru a se evita riscul de monoterapie, este preferabil
să nu se iniţieze tratamentul empiric şi să se aştepte rezultatul antibiogramei.
Faza de tratament individualizat pe baza
rezultatelor antibiogramei
Se începe după obţinerea antibiogramei fiabile (într-un
LNR). Interpretarea se va face ţinând cont de contextul clinic şi de evoluţia
bacteriologică a bolnavului. De exemplu, în cazul în care un pacient devine
negativ M şi C sub un tratament empiric, cu evoluţie clinică şi Rx favorabile,
iar antibiograma indică rezistenţă la medicamentele folosite în schemă, este
recomandabil să nu se modifice schema eficientă.
MANAGEMENTUL MEDICAMENTELOR ANTITUBERCULOASE
Managementul medicamentelor presupune 4 funcţii
fundamentale:
- selecţie - reprezintă alegerea unor medicamente de
calitate, eficiente şi cu dozaje adecvate. Se preferă în general produse cu
dozaj mare pe unitate terapeutică şi combinaţii în doze fixe;
- procurare - constă în
cuantificarea necesarului de medicamente, alegerea metodei de procurare,
organizarea licitaţiilor, stabilirea clauzelor contractuale, asigurarea
respectării termenilor
contractului de către furnizori şi asigurarea calităţii medicamentelor;
- distribuţie - include proceduri vamale în cazul medicamentelor importate, controlul stocului, managementul rezervelor şi livrarea
medicamentelor către depozitele de medicamente, unităţile sanitare şi
furnizorii de servicii de sănătate;
- utilizare -
diagnosticare, prescriere, administrare şi consum corect al medicamentului. Cele mai multe dintre medicamentele de linia I sunt utile
numai pentru tratamentul TB.
In cadrul subprogramului curativ „Tratamentul
bolnavilor cu tuberculoză" achiziţia medicamentelor şi materialelor
sanitare specifice se efectuează de către unităţile sanitare care derulează
subprogramul, în conformitate cu legislaţia în domeniul achiziţiilor publice,
în limita bugetului alocat. Sumele prevăzute cu această destinaţie sunt
asigurate din bugetul Fondului naţional unic de asigurări sociale de sănătate,
în baza contractelor încheiate distinct cu CASJ. Lista cuprinzând denumirile
comerciale ale medicamentelor pentru care nu se stabileşte preţ de referinţă,
aferente denumirilor comune internaţionale, aprobată prin hotărâre a
Guvernului, precum şi materialele sanitare specifice care se acordă bolnavilor
beneficiari ai subprogramului curativ „Tratamentul bolnavilor cu
tuberculoză" se aprobă prin ordin comun al ministrului sănătăţii publice
şi al preşedintelui CNAS. Eliberarea medicamentelor se face prin farmaciile cu
circuit închis ale unităţilor sanitare, pe bază de condică, atât pentru
tratamentul spitalicesc, cât şi pentru cel ambulatoriu.
Medicul pneumolog din ambulatoriu recomandă schema de
tratament şi prescrie lunar medicamentele pentru bolnavii aflaţi în tratament
şi săptămânal sau ori de câte ori este nevoie pentru bolnavii care intră în
tratament.
In cazul pacienţilor care primesc tratamentul la nivelul
DPF, medicamentele sunt păstrate în camera de tratament şi administrate de
către cadrul medical special instruit din DPF.
Pentru pacienţii care nu pot urma DOT la nivelul DPF
din diverse cauze, acesta este administrat sub directă observare de către o persoană
special instruită care îşi asumă responsabilitatea corectitudinii administrării
(membri ai familiei, învăţători, preoţi, asistenţi sociali din comunitate,
asistenţi medicali comunitari) sau de către MF.
MF ridică lunar, personal sau prin intermediul unui
delegat, de la DPF medicamentele antituberculoase pentru bolnavii pe care îi
are în supraveghere/tratament. Le păstrează în cabinet, în plicuri individuale,
şi le administrează sub directă observaţie, consemnând administrarea fiecărei
doze în fişa de tratament. La încheierea tratamentului, fişa de tratament
completată cu fiecare doză administrată va fi dusă la DPF.
In cadrul proiectului DOTS plus, medicamentele de linia
a II-a sunt selectate, distribuite şi utilizate după reguli care corespund
cerinţelor internaţionale ale OMS şi GLC în cadrul unui sistem propriu finanţat
de către GFATM.
Medicamentele antituberculoase
necesare realizării chimioprofilaxiei la persoanele cu risc se achiziţionează
din fonduri gestionate de MSP, prin intermediul ASPJ.
Unităţile sanitare care derulează subprogramul
„Tratamentul bolnavilor cu tuberculoză" au obligaţia gestionării eficiente
a mijloacelor materiale şi băneşti, a organizării evidenţei contabile a
cheltuielilor şi a organizării evidenţei nominale, pe baza codului numeric
personal, a beneficiarilor subprogramului.
EVALUAREA REZULTATULUI TRATAMENTULUI
Orice caz de TB înregistrat va
fi evaluat în momentul în care se cunosc toate informaţiile necesare evaluării,
dar nu mai târziu de 12 luni de la data declarării.
In momentul evaluării se completează Fişa de evaluare a
tratamentului antituberculos (anexa nr. 13, care face parte integrantă din
prezentele norme metodologice).
Tabelul 7: Categoriile de evaluare a rezultatului
tratamentului
|
Categorie
|
Descriere
|
|
Vindecat (V)
|
Pacientul cu TB pulmonară confirmată bacteriologic, care a urmat
o cură completă de tratament şi care este negativ la sfârşitul tratamentului
şi cel puţin la încă un control anterior
|
|
Tratament complet (T)
|
Pacientul care a urmat o cură completă de tratament, dar care nu
are criteriile pentru a fi evaluat ca „Vindecat" sau „Eşec" (fie nu
a fost confirmat bacteriologic, fie nu are două controale bacteriologice,
dintre care unul la sfârşitul tratamentului şi celălalt cu o ocazie anterioară,
sau localizarea bolii a fost extrapulmonară)
|
|
Eşec (E)
|
Cazul care rămâne pozitiv la examenul bacteriologic după 4 luni
de tratament corect administrat sau cazul iniţial negativ la examenul
bacteriologic şi care devine pozitiv la controlul de la terminarea fazei
intensive a tratamentului vor fi evaluate ca „Eşec".
Cazurile evaluate ca „Eşec" vor fi reînregistrate imediat ca
„Retratament pentru eşec" (sau cazuri cronice, dacă eşecul a fost
constatat în cursul sau la sfârşitul unui retratament) şi vor începe o cură
de retratament cu regimul II sau individualizat în funcţie de rezultatul antibiogramei
|
|
Abandon (A)
|
Pacientul care a întrerupt tratamentul
mai mult de două luni consecutive sau mai mult de 20% din totalul prizelor
indicate
Pacienţii cu întreruperi ale tratamentului mai scurte de două
luni vor recupera prizele omise la sfârşitul fazei de tratament în care
acestea au fost înregistrate, dar nu mai mult de 20% din numărul total al
prizelor.
|
|
Decedat (D)
|
Pacientul care decedează din orice cauză în timpul tratamentului
pentru TB
La aceste cazuri se va menţiona într-o rubrică specială cauza
decesului: TB (simbol pentru evaluare: „D") sau altă cauză (simbol pentru evaluare:
„d").
Cazurile declarate post-mortem vor fi imediat evaluate ca
„Decedat".
|
|
Mutat (M)
|
Pacientul transferat după înregistrare şi declarare, în timpul
tratamentului antituberculos, într-un alt DPF pentru continuarea tratamentului
|
|
Pierdut (P)
|
Pacientul care a abandonat tratamentul şi care nu mai este găsit
la adresa cunoscută pentru a fi recuperat
|
|
Continuă tratamentul (C)
|
Pacientul care îşi continuă tratamentul peste 12 luni
|
Pacienţii care nu au luat deloc tratament anti TB la 12
luni de la înregistrare vor fi evaluaţi ca „Abandon" sau „Pierdut".
Tabelul 8: Categoriile
de evaluare finală a pacienţilor cu MDR-TB
|
Categorie
|
Descriere
|
|
Vindecat
|
Un pacient MDR-TB care:
- a efectuat o cură completă de tratament conform protocolului
ţării (în România, programul DOTS plus prevede continuarea tratamentului încă
18 luni după conversie);
- are culturi negative în ultimele 12 luni de tratament;
- a avut minimum 5 culturi efectuate în ultimele 12 luni de
tratament
Ca excepţie, un pacient poate fi considerat
vindecat chiar dacă are numai o cultură pozitivă în acest interval, dar nu
are semne clinice sau radioscopice de activitate.
|
|
Tratament încheiat
|
Un pacient MDR-TB care a încheiat tratamentul în acord cu
protocolul DOTS plus, dar nu îndeplineşte criteriile
pentru a fi evaluat „Vindecat" sau „Eşec" datorită lipsei
rezultatelor bacteriologice
|
|
Eşec
|
Un pacient:
- cu mai mult de o cultură pozitivă în ultimele 12 luni de
tratament, dintr-un minimum de 5 culturi efectuate în
ultimele 12 luni; sau
- cu una dintre ultimele 3 culturi finale pozitivă; sau
- cu culturi persistent pozitive şi se ia decizia clinică de a
întrerupe tratamentul; sau
- la care se decide întreruperea definitivă a tratamentului
datorită intoleranţelor la medicamente
|
|
Abandon
|
Un pacient:
- care a întrerupt tratamentul pentru două luni consecutive sau
mai mult;
- căruia i s-a oprit tratamentul de către clinician datorită
numeroaselor întreruperi, mai scurte de două luni
|
|
Categorie
|
Descriere
|
|
Decedat
|
Pacientul cu MDR-TB care decedează pe
parcursul tratamentului, indiferent de cauză (pentru aceste cazuri se va
înscrie într-o rubrică specială cauza decesului: TB sau altă cauză)
|
|
Mutat
|
Pacientul cu MDR-TB care se mută într-o altă unitate teritorială
în timpul tratamentului
|
|
Pierdut
|
Pacientul cu MDR-TB care întrerupe tratamentul şi care nu mai
poate fi recuperat, întrucât nu mai locuieşte la adresa cunoscută
|
Atitudinea de urmat în caz de abandon:
• caz pozitiv la microscopie: se evaluează
tratamentul anterior ca „Abandon", se reînregistrează cazul ca
„Retratament după abandon" şi se începe o nouă cură de tratament;
• caz negativ la microscopie:
- pozitiv la cultură: se evaluează tratamentul
anterior ca „Abandon", se reînregistrează ca „Retratament după
abandon" şi se începe o nouă cură de tratament;
- negativ la cultură: se menţine în observaţie prin
control bacteriologic cel puţin trimestrial timp de un an şi ori de câte ori
este nevoie.
Dacă microscopia sau cultura se pozitivează, se reînregistrează
ca „Retratament după abandon" şi se începe un nou tratament.
PREVENŢIA TB
1. Vaccinarea BCG
Vaccinarea BCG este o
metodă de imunizare activă prin care se realizează o profilaxie
antituberculoasă relativă, care nu împiedică infectarea cu MT şi nici nu
întrerupe lanţul epidemiologie al bolii.
Indicaţiile vaccinării
In România BCG vizează obligatoriu doar nou-născuţii.
Vaccinarea se efectuează nediscriminatoriu la toţi nou-născutii, la vârsta de 4-7 zile (dacă nu există
contraindicaţii), înainte de externarea din maternitate şi fără testare
tuberculinică prealabilă. Dacă din diverse motive nou-născutul nu a putut fi
vaccinat în maternitate şi nu prezintă contraindicaţii, urmează să fie
recuperat vaccinai de către MF, până la vârsta de 3 luni, fără testare
tuberculinică.
Controlul formării cicatricei postvaccinale BCG se
efectuează după vârsta de 6 luni a sugarului de către MF, cu ocazia
examinărilor de bilanţ. Repetarea vaccinării nu se justifică. Revaccinarea s-a
sistat în România din anul 1998.
Tehnica vaccinării BCG este detaliată în anexa nr. 14,
care face parte integrantă din prezentele norme metodologice.
2. Chimioprofilaxia
Scopul chimioprofilaxiei TB este de a împiedica
dezvoltarea unei TB active la persoanele care au venit în contact cu o sursă de
infecţie (bolnav cu TB pulmonară cu microscopie pozitivă).
Se adresează în special copiilor, adolescenţilor (12-16
ani) şi tinerilor (până la 19 ani).
In stabilirea indicaţiilor de administrare a
chimioprofilaxiei se ţine cont de următoarele criterii de interpretare a
testului cutanat la PPD (tabelul nr. 9), dar şi de vârsta şi starea de
imunitate ale persoanei examinate.
Tabelul 9: Interpretarea testului cutanat la PPD
|
Dimensiuni
|
Rezultatul intradermoreacţiei
|
|
< 5 mm
|
negativ
|
|
5-9 mm
|
negativ în general, dar:
- pozitiv: subiecţi cu HIV/SIDA
- îndoielnic: contact recent şi repetat cu un caz de TB pulmonară
BK+
|
|
10-17 mm
|
pozitiv, dacă este un factor de risc
|
|
> 18 mm
|
pozitiv
|
Indicaţiile chimioprofilaxiei:
Primul pas este excluderea TB active.
a) Nou-născuţii din focarul
de TB - pentru
detalii se va consulta „Ghidul diagnosticului TB la copil", cap. IV
b) Copii 0-14 ani:
- cei cu IDR pozitiv, timp de cel puţin 6 luni;
- cei cu IDR negativ sau îndoielnic, timp de 3 luni,
apoi repetă IDR. In caz de viraj tuberculinic (IDR pozitiv), chimioprofilaxia
se continuă până la cel puţin 6 luni, iar în caz de IDR negativ, se întrerupe
numai dacă dispare sursa de contagiune (negativare bacteriologică sau izolare).
c) Adolescenţi şi adulţi
până la 35 de ani, numai la persoanele care prezintă factori de risc şi au IDR
pozitiv:
- boli imunosupresoare (leucemii, limfoame, boala
Hodgkin, imunodeficienţe câştigate sau dobândite);
- imunosupresie medicamentoasă (chimioterapie
anticanceroasă, steroizi);
- insuficienţă renală cronică;
- pneumoconioze;
- diabet zaharat insulino-dependent prost controlat;
- sindrom de malabsorbţie, subnutriţie cronică, ulcer
duodenal cronic;
- gastrectomizaţi, în special cei cu nutriţie proastă.
Chimioprofilaxia constă în monoterapie cu Izoniazidă (H), administrată zilnic (7/7), 10 mg/kgc/zi
sau 200mg/m2
suprafaţă corporală la copii, 5 mg/kgc/zi la adulţi (maximum 300 mg/zi) timp de
cel puţin 6 luni. Fişa pentru chimioprofilaxie este prezentată în anexa nr. 15,
care face parte integrantă din prezentele norme metodologice.
In cazul unui contact cu sursă bK H rezistentă poate fi
luată în considerare profilaxia şi cu alte medicamente antituberculoase decât
Izoniazidă.
Chimioprofilaxia dublă sau cu mai multe medicamente
este, în principiu, interzisă.
La profilaxia medicamentoasă se
recomandă asocierea Piridoxinei (vitamina B6), 250 mg/zi, în special la copiii alăptaţi la sân, copiii cu dietă
carenţială proteică, infectaţii cu HIV, persoanele cu boli care predispun la
neuropatii.
Chimioprofilaxia la contacţii HIV negativi ai
pacienţilor cu MDR-TB
Nu există un consens internaţional privind indicaţiile
şi schemele terapeutice folosite pentru tratamentul chimioprofilactic al
contacţilor pacienţilor cu MDR-TB.
In cazul contacţilor cu risc mare de progresie a
infecţiei latente cu germeni multidrog rezistenţi spre boală (status imunitar
deficitar), se recomandă administrarea tratamentului chimioprofilactic, în timp
ce în cazul contacţilor imunocompetenţi poate fi luată în consideraţie numai
supravegherea fără tratament timp de minimum 2 ani.
Regimurile recomandate de chimioprofilaxie:
- Pirazinamida (25-30 mg/kgc/zi) plus Etambutol (15-25
mg/zi);
- Pirazinamida (25-30 mg/kgc/zi) plus o quinolonă cu
activitate antituberculoasă (Ciprofloxacin, Ofloxacin sau Levofloxacin).
Durata recomandată: 12 luni
pentru imunodeprimaţi şi cel puţin 6 luni pentru imunocompetenţi.
3. Controlul
transmiterii infecţiei tuberculoase
Măsuri generale de prevenire a infecţiei:
- tratamentul prompt al bolnavilor diagnosticaţi;
- igiena tusei;
- diluţia bacililorîn atmosferă: ventilaţie eficientă,
lumină naturală (radiaţia solară), radiaţia ultravioletă.
Măsuri speciale în unităţile de îngrijire a bolnavilor
de TB:
- spitalizarea bolnavilor cu TB pulmonară cu microscopie
pozitivă, în faza intensivă, în condiţii adecvate de habitat;
- doar pacienţii cu TB confirmată pot fi admişi în
secţia de TB;
- pacienţii cu TB vor fi izolaţi de ceilalţi pacienţi
cu afecţiuni pulmonare; în cazul în care pacienţii cu TB se deplasează în
spaţii comune sau în alte secţii, vor purta măşti chirurgicale pentru evitarea
contaminării aerului în zonele vizitate;
- se va evita contactul persoanelor infectate cu HIV
cu bolnavi de TB, în special cu cei cu microscopie pozitivă;
- personalul medical va folosi obligatoriu măşti de
protecţie a respiraţiei, conform recomandărilor OMS şi ECDC, în special în
zonele cu risc crescut (camere de recoltare a sputei, saloane cu pacienţi
contagioşi, laborator, în timpul procedurilor producătoare de aerosoli,
servicii de bronhologie);
- recoltarea sputei se va face
în spaţii special amenajate şi în recipiente de unică folosinţă care ulterior
se incinerează;
- vor fi asigurate ventilaţia adecvată, naturală sau
artificială, pentru toate spaţiile în care sunt internaţi bolnavi cu TB şi flux
de aer dirijat şi filtru HEPA, pentru spaţiile în care sunt internaţi bolnavi
cu MDR-TB;
- desemnarea unor persoane din unitate care vor fi
responsabile de constituirea şi menţinerea unui program de control al infecţiei
tuberculoase (Ordinul ministrului sănătăţii publice nr. 916/2006 privind
aprobarea Normelor de supraveghere, prevenire şi control al infecţiilor
nosocomiale în unităţile sanitare);
- dezinfecţia chimică a aerului şi a suprafeţelor
potenţial contaminante se va face conform Ordinului ministrului sănătăţii
publice nr. 261/2006 pentru aprobarea Normelor tehnice privind curăţarea,
dezinfecţia şi sterilizarea în unităţile sanitare.
INTERVENŢII PENTRU SCHIMBAREA COMPORTAMENTELOR
MSP în colaborare cu INPMN şi institutele de sănătate
publică coordonează activităţile de IEC, elaborate pe baza experienţei
specifice a României; eficienţa acestora poate spori, dacă alături de organele de decizie guvernamentale sunt implicate,
în vederea adoptării unor comportamente favorabile sănătăţii, şi organizaţii
neguvernamentale, foşti pacienţi, reprezentanţi ai comunităţii, întreprinzători
particulari. La nivelul judeţelor această responsabilitate revine managerilor
judeţeni ai PNCT, care vor avea sprijinul compartimentelor de promovare a
sănătăţii de la nivelul ASPJ.
Materiale IEC care pot fi
utilizate vor fi disponibile pe site-ul MSP şi INPMN, urmând a fi publicate şi
difuzate gratuit în funcţie de necesităţi. Acestea pot include: „Ghidul
pacientului TB (copii)" şi „Ghidul pacientului TB (adulţi)", pliante,
broşuri, postere etc.
Ziua mondială de luptă împotriva TB
In fiecare an, la data de 24 martie, se va marca Ziua
mondială de luptă împotriva TB, urmând tematica propusă de OMS. Minimal se va
organiza o conferinţă de presă la nivel central şi judeţean pentru prezentarea
situaţiei curente a endemiei TB şi pentru obţinerea sprijinului comunităţii în
vederea rezolvării dificultăţilor întâmpinate. In funcţie de bugetul disponibil
se pot organiza şi alte activităţi (concursuri, distribuţie de pliante şi
broşuri etc).
Intervenţia prin
mass-media
Se vor populariza/publica materiale educative
referitoare la TB în ziare şi reviste, se vor prezenta la radio emisiuni cu
aceeaşi temă, se va introduce şi extinde transmiterea pe mai multe canale de
televiziune a unor filme de scurt metraj sau spoturi publicitare având ca
mesaje depistarea şi tratamentul corect al TB.
Tot prin intermediul mass-mediei trebuie schimbată
atitudinea reticentă a colectivităţii faţă de pacienţii cu TB. Comunitatea
trebuie să fie mobilizată pentru a interveni în sprijinul pacienţilor prin
suport psihologic, prin acte de caritate; dacă se evită stigmatizarea şi
marginalizarea socială, există şansa obţinerii unei complianţe depline.
Cu sprijinul compartimentelor de promovare a sănătăţii
de la nivelul ASPJ se vor multiplica afişele, posterele, calendarele, pliantele
tematice deja existente şi se vor concepe altele noi.
Se va avea în vedere organizarea unor acţiuni specifice
pentru grupurile vulnerabile (romi, persoane fără adăpost, deţinuţi etc).
Site-ul web www.tuberculoza.ro va
fi întreţinut periodic, fiind adăugate informaţii utile pentru pacienţi şi
familiile acestora. Se va face publicitate site-ului prin anunţuri în cotidiene
şi broşuri de publicitate.
Aderenţa pacientului la tratament
Aderenţa la tratament înseamnă
că un pacient urmează cu stricteţe terapia recomandată, luând toate
medicamentele prescrise pe întreaga durata a acesteia. Aderenţa este importantă
deoarece TB este aproape întotdeauna curabilă dacă pacientul urmează tratamentul.
Nonaderenţa reprezintă
refuzul sau incapacitatea pacientului de a lua medicamentele prescrise conform
instrucţiunilor. Acest comportament reprezintă cea mai mare problemă în
controlul TB şi poate avea consecinţe grave.
Un pacient neaderent la tratament poate:
- avea o durată mai lungă a bolii sau o boală mai
severă;
- transmite TB altora;
- dezvolta şi transmite o MDR-TB;
- deceda ca urmare a întreruperii tratamentului.
Pacienţii şi personalul sanitar sunt în egală măsură responsabili pentru asigurarea aderenţei
la tratament. Decizia pacientului şi a familiei de a administra sau nu
medicamentele depinde în foarte mare măsură de ajutorul pe care îl primesc sau
nu din partea personalului sanitar atunci când îl solicită. Educaţia
pacientului este vitală.
Rolul reţelei medicale în diminuarea nonaderenţei la
tratamentul anti TB
Personalul sanitar, medicii, asistenţii medicali din
reţeaua de pneumologie, MF, asistenţii medicali ai MF şi asistenţii medicali
comunitari trebuie să îşi rezerve timp pentru a explica, în mod repetat, în
limbaj simplu, câte medicamente trebuie luate şi când şi să se asigure că
explicaţiile au fost înţelese. Dialogul, participarea pacientului la discuţii
reprezintă elemente-cheie ale comunicării interpersonale. Această activitate
trebuie desfăşurată atât în cursul spitalizării, cât şi în faza de continuare a
tratamentului în ambulatoriu.
Aceleaşi mesaje pot fi transmise, atât în spitale, cât
şi în ambulatorii, prin intermediul unor sisteme de radioficare cu circuit
intern.
In anexa nr. 16, care face parte integrantă din
prezentele norme metodologice, sunt prezentate pe scurt ideile principale
pentru discuţia cu pacienţii la diferite momente ale tratamentului şi în
situaţii particulare. Informaţiile cuprinse în anexa amintită pot fi tipărite
pentru a servi ca aide-memoire personalului sanitar.
Un rol important în evaluarea gradului şi cauzelor de
noncomplianţă îl au psihologii, a căror intervenţie - consult şi sfat
psihologic repetat - poate fi esenţială în descoperirea riscului de nonaderenţă
la tratament şi în diminuarea acestui tip comportamental.
Intervenţia serviciilor de asistenţă socială
Serviciile de asistenţă socială din cadrul
administraţiilor publice locale vor fi implicate în acest tip de acţiuni IEC.
Asistenţii sociali, a căror prezenţă în structura de
supraveghere şi control al TB este necesară, pot interveni, după efectuarea
anchetelor sociale, în sprijinul financiar al pacientului (obţinerea de
ajutoare sociale, pensii de invaliditate, ajutoare de handicap), în plasarea
pacienţilor fără domiciliu în aşezăminte medico-sociale; scopul acestor
demersuri este de a spori aderenţa la tratament a bolnavilor de TB. Pot fi
folosite stimulente sub forma bonurilor valorice pentru alimente, distribuite
de către asistenţii sociali în colaborare cu medicii pneumologi numai
pacienţilor care urmează DOT în ambulatoriu.
Sprijinul oferit de mediatorii comunitari poate fi
esenţial în diminuarea noncomplianţei pacienţilor la tratament.
Suportul confesional, oferit prin intermediul preoţilor care îşi desfăşoară activitatea în spitale, nu trebuie
neglijat în prevenirea abandonului tratamentului.
DEZVOLTAREA RESURSELOR UMANE
Scopul pe termen lung al dezvoltării resurselor umane
pentru controlul TB este de a se ajunge la situaţia în care personalul de la
diferite niveluri ale sistemului de sănătate dobândeşte abilităţile,
cunoştinţele şi atitudinea necesare (cu alte cuvinte, este competent) pentru a
implementa cu succes şi a susţine activităţile de control al TB, inclusiv
pentru a implementa strategii noi, revizuite. Fără atingerea şi menţinerea
acestui scop nu va fi posibil să se atingă si să se susţină ţintele globale de
control al TB.
Dezvoltarea resurselor umane este parte integranta a
PNCT.
Obiective:
- îmbunătăţirea programelor existente de formare în controlul TB;
- identificarea deficienţelor de performanţă generate
de lipsa de cunoştinţe sau de abilităţi;
- identificarea personalului nou-intratîn sistem şi
facilitarea accesului acestuia la programe de formare corespunzătoare;
- revizuirea periodică a
programei universitare a medicilor, precum şi a celei a asistenţilor medicali
pentru a se asigura că noii absolvenţi sunt pregătiţi să lucreze în domeniul
controlului TB, inclusiv în cadrul laboratoarelor bK;
- corelarea formării pentru
controlul TB cu formarea pentru controlul HIV/SIDA.
Activităţi:
- constituirea unui grup de coordonare a formării din
reprezentanţi ai instituţiilor de învăţământ, ai personalului din teren, ai
organizaţiilor profesionale;
- evaluarea nevoilor de formare
în funcţie de setul-standard de performanţă a activităţii şi de fişele de post
şi analiza datelor pentru stabilirea domeniilor care necesită a fi
îmbunătăţite;
- pregătirea planurilor de formare pe termen scurt
(anuale) şi mediu, incluzând obiectivele şi activităţile necesare pentru
atingerea fiecărui obiectiv;
- organizarea cursurilor de formare la nivel central,
regional şi judeţean;
- pregătirea propunerilor de buget pentru activităţile
de formare, controlul şi managementul fondurilor, monitorizarea cheltuielilor,
raportare financiară, utilizarea rapoartelor financiare pentru luarea deciziei;
- evaluarea implementării planului de formare
(evaluarea procesului deformare, evaluarea rezultatelor formării, revizuirea
planului de formare conform rezultatelor monitorizării şi evaluării);
- asigurarea colaborării cu organizaţii profesionale în
vederea obţinerii creditelor pentru educaţie medicală continuă;
- asigurarea legăturii cu organizaţii şi agenţii
internaţionale pentru accesul la asistenţă tehnică şi financiară pentru formare
şi participarea la cursuri de formare la nivel internaţional pentru
personalul-cheie implicat în PNCT.
Formatorii:
- cadre universitare de la nivelul universităţilor de
medicină şi farmacie şi al colegiilor pentru asistenţi medicali;
- profesionişti din domeniul pneumologiei special
pregătiţi pentru formarea continuă a personalului prin cursuri de formare
deformatori;
- profesionişti în domeniul medicinei de laborator
special pregătiţi pentru formarea continuă a personalului prin cursuri de formare de formatori.
Cum este organizată formarea:
- la nivel universitar, în cadrul disciplinei
Pneumologie, şi la nivelul colegiilor pentru asistenţi medicali;
- la nivel postuniversitar, prin cursuri scurte
organizate la nivel central, regional şi judeţean;
- prin studiu individual folosind instrumente ale
învăţământului la distanţă (site web, CD-uri educaţionale etc).
CERCETAREA
Se va urmări furnizarea către CTJ ai PNCT a
informaţiilor şi oportunităţilor pe care ei le pot folosi pentru a lua acele
decizii care să îmbunătăţească performanţele PNCT. Se va acorda prioritate
următoarelor teme de cercetare:
1. analiza cost-beneficiu în managementul bolnavului de
TB în cadrul aplicării strategiei DOTS;
2. evaluarea impactului vaccinării asupra endemiei TB în România;
3. identificarea tulpinilor de micobacterii şi punerea
în evidenţă a rezistenţei multiple prin genotipare sau metode fenotipice
rapide;
4. metode neconvenţionale în diagnosticul TB: IGRA, PCR
etc;
5. valoarea examenului bacteriologic din prelevatele obţinute prin bronhoscopie;
6. valoarea examenului bacteriologic în funcţie de
calitatea sputei examinate;
7. studiu privind cauzele nonaderenţei la tratamentul
antituberculos si metode de ameliorare;
8. studiul caracteristicilor endemiei
TB în grupurile populaţionale vulnerabile;
9. supravegherea evoluţiei chimiorezistenţei la MT la
nivel naţional;
10. controlul extern al calităţii antibiogramei pentru
medicamentele de linia I şi
linia a II-a.
SUPERVIZAREA
Este o activitate importantă,
continuă, sistematică. Utilizează mijloace specifice şi ajută persoanele care
îşi desfăşoară activitatea în domeniul controlului TB să îşi îmbunătăţească
performanţele prin ameliorarea cunoştinţelor, abilităţilor şi a atitudinilor,
precum şi a motivaţiei pentru munca desfăşurată.
Urmăreşte respectarea recomandărilor cuprinse în PNCT,
identificarea cât mai precoce a dificultăţilor întâmpinate şi a eventualelor
erori în implementarea activităţilor şi formulează recomandări în vederea
creşterii performanţei PNCT.
Este organizată pe diferite niveluri:
- de la nivelul unităţii centrale a PNCT la judeţe;
- de la unităţile judeţene ale PNCT la unităţile
teritoriale. Sunt urmărite în paralel şi integrate două aspecte importante legate de activităţile de control al TB:
- activităţile de diagnostic, tratament, monitorizare a
cazurilor de TB şi de supraveghere epidemiologică a TB în teritoriu;
- activitatea laboratoarelor de bacteriologie bK:
folosirea tehnicilor standardizate şi controlul calităţii diagnosticului bacteriologic al TB.
Este efectuată de către supervizori, membri ai Comisiei
de supervizare-monitorizare a implementării PNCT, denumită în continuare Comisia de supervizare, pentru
unităţile de pneumoftiziologie, şi de către membrii Grupului de lucru pentru laboratoare bK, pentru laboratoarele de bacteriologie bK.
Supervizorii sunt medici pneumologi, respectiv personal
cu pregătire superioară din laboratoarele de bacteriologie bK, cu preocupări şi
rezultate deosebite în domeniul activităţilor de control al TB şi
disponibilitate de a efectua această activitate, şi sunt numiţi prin ordin al
ministrului sănătăţii publice, la propunerea CTN al PNCT.
Vizitele de supervizare de la UCM la judeţe pentru
unităţile de pneumoftiziologie se desfăşoară după cum urmează:
- sunt efectuate de către 2-3 membri ai Comisiei de
supervizare, la nivelul fiecărui judeţ/sector din municipiul Bucureşti, de două
ori pe an sau ori de câte ori este nevoie; planificarea acestor vizite este
efectuată de către coordonatorul Comisiei de supervizare. Unităţile care
urmează să fie vizitate vor fi anunţate cu cel puţin 10 zile anterior
efectuării vizitei;
- sunt vizitate toate unităţile care desfăşoară
activităţi legate de controlul TB: DPF, spitalele/secţiile de
pneumoftiziologie, laboratoarele de bacteriologie bK;
- se completează chestionarele specifice fiecărui tip
de unitate, care sunt actualizate periodic (anual), în funcţie de rezultatele
înregistrate şi problemele identificate la nivel naţional; aceste chestionare
sunt elaborate de către membrii Comisiei de supervizare şi sunt acceptate de
comun acord - ele constituie instrumentul de lucru pentru efectuarea acestor
vizite;
- pe lângă culegerea de informaţii referitoare la
activităţile de control al TB, supervizorii au rolul de a informa şi îndruma
personalul din unităţile de pneumoftiziologie în legătură cu activităţile de
control al TB;
- la sfârşitul vizitei ASPJ este informată de către
membrii Comisiei de supervizare asupra principalelor constatări şi recomandări
de ameliorare a activităţilor de control al TB din judeţ;
- se redactează un raport narativ care conţine aceste
constatări si recomandări si care se trimite ulterior la UCM a PNCT,
laASP-MSPşi la ASPJ.
Vizitele de supervizare de la unitatea judeţeană la
unităţile teritoriale se desfăşoară după cum urmează:
- sunt efectuate de către CTJ al PNCT, trimestrial sau
ori de câte ori este nevoie, la toate DPF din judeţ;
- se completează un chestionar specific, elaborat şi
acceptat de comun acord de către membrii Comisiei de supervizare;
- se realizează informarea şi îndrumarea colegilor din
teritoriu asupra activităţilor de control al TB;
- se formulează recomandări care sunt înaintate ASPJ şi
managerului unităţii de care aparţine DPF respectiv;
- în baza arondării teritoriale a MF la medicii
specialişti pneumologi care îşi desfăşoară activitatea în DPF, aceştia vor
efectua vizite de supervizare la cabinetele individuale ale MF de două ori pe
an sau ori de câte ori este nevoie; se completează un chestionar specific.
Vizitele de supervizare pentru
laboratoarele de bacteriologie bK se desfăşoară după cum urmează:
- constituie o componentă importantă a controlului
calităţii diagnosticului bacteriologic al TB;
- anual, fiecare laborator judeţean de bacteriologie bK
este vizitat de către un membru al Grupului de lucru pentru laboratoare al
PNCT. Planificarea acestor vizite este în responsabilitatea coordonatorului
reţelei naţionale de laboratoare de bacteriologie bK;
- se completează un chestionar specific, care urmăreşte
toate aspectele relevante care ar putea influenţa rezultatele examenului
bacteriologic (probleme de personal, tehnici de lucru, controlul calităţii
diagnosticului, măsuri de control al infecţiilor în cadrul laboratorului);
chestionarul este elaborat şi acceptat de comun acord de către membrii Grupului
de lucru pentru laboratoarele de bacteriologie bK al PNCT;
- fiecare responsabil judeţean pentru laboratoarele de
bacteriologie bK vizitează de două ori pe an sau ori de câte ori este nevoie
toate laboratoarele de bacteriologie bK din judeţ; efectuează controlul extern
al calităţii diagnosticului bacteriologic şi îndrumarea metodologică a
colegilor din laboratoarele vizitate.
Se urmăreşte şi modalitatea de comunicare a unităţilor
de pneumoftiziologie între ele, cu laboratoarele de bacteriologie bK, cu CTN al
PNCT, precum şi cu alte instituţii, programe, categorii profesionale implicate
în activităţile de control al TB: epidemiologi, MF, penitenciare, Programul de
control al HIV/SIDA, asistenţi comunitari, mediatori medicali, primării,
organizaţii neguvernamentale care îşi desfăşoară activitatea în teritoriu etc.
Urmărirea respectării recomandărilor cuprinse în
raportul vizitei de supervizare este responsabilitatea CTJ al PNCT si a ASPJ.
Concluziile rezultate în urma acestor vizite vor fi
cuprinse într-un raport anual realizat la nivelul Comisiei de supervizare, care
va fi înaintat ASP-MSP.
MANAGEMENTUL CIRCUITULUI INFORMAŢIONAL
Circuitul informaţional al datelor privind TB se
efectuează atât în sistem clasic, pe suport hârtie, cât si electronic,
printr-un soft special destinat colectării datelor privind TB. Ambele căi au
avantaje si dezavantaje şi se completează reciproc.
Pentru înregistrarea în format electronic a datelor se
utilizează:
- sistemul informaţional „Supravegherea epidemiologică
a TB şi monitorizarea PNCT" în Microsoft SQL Server, denumită în
continuare soft; şi
- baza naţională de date din Fox Pro.
Pentru ca sistemul informaţional să fie operativ este
necesar ca toate unităţile din reţeaua de pneumoftiziologie să completeze şi să
transmită corect, complet şi în termenele stabilite mai jos informaţiile
solicitate conform formularelor-standard cuprinse în anexele nr. 9-13, care fac
parte integrantă din prezentele norme metodologice. In conformitate cu
prevederile Hotărârii Guvernului nr. 589/2007 pentru aprobarea circuitului
informaţional al fişei unice de raportare a bolilor transmisibile, pentru
înregistrarea/circularea şi transmiterea datelor privind TB vor fi folosite
fişele specifice prevăzute în anexele nr. 4, 7, 9, 10, 12, 13, 15 şi 17, care
fac parte integrantă din prezentele norme metodologice.
Toate DPF care aparţin de MSP, precum şi unităţile care
joacă rolul dispensarelor TB din MJ, MAşi MIRA introduc în soft datele de luare
în evidenţă, monitorizare şi evaluare ale fiecărui pacient înregistrat în
Registrul de TB. In momentul luării în evidenţă a unui pacient, din soft se
tipăreşte automat fişa de declarare a cazului; în momentul evaluării se
tipăreşte fişa de evaluare, iar în momentul transferului -fişa de transfer.
Fişele de declarare, semnate şi parafate de către
medicul care a luat cazul în evidenţă, sunt trimise CTJ al PNCT, care le
centralizează şi le duce la ASPJ în prima zi lucrătoare a lunii, pentru luna
precedentă. Apoi, după maximum 5 zile lucrătoare, acestea sunt trimise la
INPMN, de preferinţă cu maşina destinată activităţilor PNCT sau prin poştă.
Fişele de evaluare, semnate şi parafate de către
medicul care a avut în evidenţă cazul, pentru cazurile de TB luate în evidenţă
cu 13 luni în urmă sunt trimise CTJ, care le centralizează şi le trimite
împreună cu declarările din luna precedentă tot la INPMN.
Atât fişele de declarare, cât şi cele de evaluare vor
fi însoţite de câte un borderou care să evidenţieze:
- pentru declarări: numărul de cazuri noi, recidive,
retratamente pentru abandon, eşecuri, cronici, numărul de „K" („Continuă
tratamentul") şi numărul cazurilor preluate prin transfer; se va menţiona
numărul copiilor cuprinşi în declararea lunii respective.
Vârsta unui pacient este calculată din diferenţa în ani
întregi dintre data începerii tratamentului (sau data declarării pentru
pacienţii care nu au luat tratament) şi data naşterii. Categoria „Copii"
cuprinde cazurile cu vârsta între 0 şi 14 ani inclusiv (dacă pacientul are 15
ani împliniţi la data începerii tratamentului antituberculos sau la data
declarării, este considerat adult);
- pentru evaluări: numărul de cazuri vindecate, cu
tratament complet, cu abandon, eşec, deces prin TB („D"), deces în timpul
tratamentului, dar cu alte cauze decât TB („d"),
evaluate „Mutat" sau „Pierdut" sau „Infirmat".
Circuitul fişei de transfer se regăseşte în anexa nr.
9.
La INPMN datele din fişele de declarare pentru anul în
curs şi din fişele de evaluare din anul precedent sunt introduse în Fox-Pro.
Din baza de date astfel constituită se pot efectua raportări avansate în
Fox-Pro şi Epi-lnfo şi exportări în TESSy.
Noul soft pentru colectarea datelor privind TB este o
aplicaţie proiectată pentru web, iar utilizatorii lucrează în pagini web
accesate prin internet direct de pe server.
Aplicaţia special creată pentru gestionarea datelor
privind TB este structurată pe 3 niveluri:
• nivelul primar, unde sunt colectate datele, la DPF şi
laboratoarele bK;
• nivelul intermediar, dispensarul judeţean unde
funcţionează UJ;
• nivelul central, UC.
Datele introduse de către nivelul DPF apar instantaneu
la nivel intermediar (UJ) şi central (UC).
CTJ al PNCT vizualizează datele introduse de către
DPF-urile din teritoriul său, efectuează raportări şi validează rezultatele la
tratament. Recordurile care conţin greşeli/omisiuni, precum şi cazurile
evaluate incorect sunt invalidate. CTJ ia legătura cu DPF-ul în cauză, care
face corecturile.
UC poate vizualiza toată situaţia pe ţară global, pe judeţe
şi pe dispensare şi poate efectua raportări. Identifică recorduri incorecte/cu
omisiuni şi ia legătura cu CTJ şi cu DPF-ul respectiv pentru corecturi.
Toate datele apărute pe parcursul monitorizării unui
pacient (internări, modificări ale tratamentului, prize omise, reacţii adverse,
rezultate ale controalelor bacteriologice, infirmare, transfer, evaluare etc.)
vor fi operate cât mai repede atât în Registrul de TB, cât şi în calculator şi
vor fi disponibile în server, la toate cele 3 niveluri.
Aplicaţia oferă posibilitatea furnizării unor rapoarte
agregate trimestriale şi anuale privind date legate de morbiditate,
investigaţii bacteriologice şi tratamente la toate cele 3 niveluri.
Datorită faptului că datele sunt disponibile în mod
operativ la toate cele 3 niveluri: local, judeţean şi central, măsurile
corective care se impun pot fi luate mult mai rapid.
Situaţiile trimestriale şi anuale referitoare la
endemia TB la nivel naţional vor fi disponibile tuturor medicilor pneumologi cu
ocazia sesiunilor de comunicări ale INPMN, publicate în revista
„Pneumoftiziologia" şi pe site-ul INPMN.
Circuitul informaţional al cazurilor de MDR/XDR-TB
Cazurile de MDR-TB sunt anunţate, declarate şi
înregistrate atât în Registrul de TB, cât şi în soft.
In momentul confirmării diagnosticului de MDR-TB, în
soft se deschide un câmp special pentru MDR-TB, unde se vor înscrie date
suplimentare faţă de datele deja înscrise pentru un caz obişnuit, atât la
înregistrare, cât şi la monitorizare şi evaluare. Astfel, se va menţiona dacă pacientul
este fost deţinut, consumator de alcool, dacă locuieşte singur sau cu alte
persoane în casă, gradul de aglomerare al locuinţei. Se va menţiona sursa de
provenienţă a medicaţiei: PNCT sau GLC. Pe lângă monitorizarea bacteriologică
se va consemna şi monitorizarea clinică, a greutăţii corporale şi evoluţia
radiologică.
Cazurile de MDR/XDR-TB pot fi introduse în aplicaţie
atât de la DPF, cât şi de la cele două centre de excelenţă pentru MDR-TB de la
Bucureşti şi Bisericani. In momentul în care un pacient se internează sau se
externează în unul/din unul dintre centrele de excelenţă, în soft se va proceda
la transferarea cazului repectiv, întocmai ca pentru transferarea unui caz
între două DPF. Validarea evaluării rezultatului tratamentului unui caz de MDR/XDR-TB
care a fost internat în unul dintre centrele de excelenţă se face de către
centrul respectiv, şi nu de către CTJ.
Cazurile introduse în soft la nivelul DPF vor fi
automat vizualizate şi de cele două centre de excelenţă pentru MDR-TB de la
Bucureşti şi Bisericani. Acestea vor întocmi Registrul naţional al cazurilor de
MDR/XDR-TB.
RAPORTĂRI STATISTICE
Periodic (lunar, trimestrial şi anual) sunt prezentate
diverse rapoarte agregate birourilor de statistică din cadrul ASPJ sau ASP-MSP,
Centrului Naţional pentru Organizarea şi Asigurarea Sistemului Informaţional şi
Informatic în Domeniul Sănătăţii Bucureşti şi CASJ.
„Evidenţa bolnavilor cu TB"
UC şi UJ raportează trimestrial şi anual indicatorii de
morbiditate (incidenţa globală, incidenţa cazurilor noi şi a recidivelor,
incidenţa îmbolnăvirilor de TB în rândul populaţiei infantile) de la nivel
naţional şi pentru fiecare judeţ către ASPJ, respectiv ASP-MSP şi Centrului
Naţional pentru Organizarea şi Asigurarea Sistemului Informaţional şi
Informatic în Domeniul Sănătăţii Bucureşti.
Termen de predare: data de 31 a
lunii care urmează trimestrului analizat.
La nivel judeţean, situaţia pentru anul precedent va fi
predată până la data de 31 ianuarie la ASPJ.
La nivel naţional, situaţia pentru anul precedent va fi
predată până la data de 31 martie atât la ASP-MSP, cât şi la Centrul Naţional
pentru Organizarea şi Asigurarea Sistemului Informaţional şi Informatic în
Domeniul Sănătăţii Bucureşti.
„Prevalenta instantanee a bolnavilor aflaţi în
tratament la 31 decembrie"
Cuprinde toate cazurile care la data respectivă se află în tratament (cele la care nu a fost completată
data încheierii tratamentului). Această prevalentă oferă valori apropiate
prevalentei bolnavilor cu TB aflaţi în evidenţă la momentul respectiv, în
condiţii normale de supraveghere epidemiologica a teritoriului (fără abandonuri
terapeutice, pierduţi din tratament sau cronici cu polichimiorezistenţă,
lipsiţi de şansă terapeutică). Termen de predare: data de 31 ianuarie, pentru
anul precedent, la Centrul Naţional pentru Organizarea şi Asigurarea Sistemului
Informaţional şi Informatic în Domeniul Sănătăţii Bucureşti.
„Evaluarea rezultatelor tratamentelor
antituberculoase administrate bolnavilor cu TB înregistraţi în anul
precedent"
Se completează la sfârşitul anului ce succedă pe cel
pentru care se efectuează evaluarea, oferind posibilitatea calculării ratei de
succes terapeutic, unul dintre indicatorii relevanţi asupra modului în care se
aplică în teritoriu măsurile prevăzute în PNCT Se calculează de asemenea rata
de eşec terapeutic, de abandon terapeutic, de deces pe perioada tratamentului
(datorat TB sau având alte cauze), de mutări din teritoriu şi de pierderi din
observaţie.
Ratele respective se calculează diferenţiat, pe
categorii de bolnavi, în funcţie de localizare şi de confirmarea
bacteriologică, prin raportare la numărul pacienţilor evaluabili, adică la
diferenţa dintre numărul pacienţilor înregistraţi şi cel al cazurilor
infirmate.
La nivel judeţean, situaţia va fi predată până la data
de 31 ianuarie la ASPJ.
La nivel naţional, situaţia pentru anul precedent va fi
predată până la data de 31 martie atât la ASP-MSP, cât şi la Centrul Naţional
pentru Organizarea şi Asigurarea Sistemului Informaţional şi Informatic în
Domeniul Sănătăţii Bucureşti, pentru perioada analizată sus-menţionată.
Indicatorii
subprogramului „Supravegherea şi controlul tuberculozei": indicatorii
fizici şi de eficienţă sunt trimişi trimestrial,
iar indicatorii fizici, de eficienţă şi de rezultat sunt trimişi anual
atât de către UJ, cât şi de către UC către ASPJ, respectiv ASP-MSP. UJ vor
trimite situaţiile sus-menţionate în termen de 5 zile lucrătoare ale lunii care
urmează trimestrului/anului analizat, concomitent atât ASPJ, cât şi INPMN.
INPMN va transmite situaţiile respective către ANP a MSP în termen de 10 zile
lucrătoare ale lunii care urmează trimestrului/anului analizat.
„Darea de seamă privind principalii indicatori ai
cunoaşterii sănătăţii"
Se completează trimestrial de către DPF numai cap. II „Morbiditate" pct. 1 „Evidenţa
bolnavilor cu TB", cu numărul cazurilor noi şi cel al recidivelor
înregistrate în trimestrul respectiv, pe tipuri de cazuri, copii/adulţi,
urban/rural, şi se trimite la ASPJ. Numărul de cazuri noi raportate de către
DPF pentru trimestrul respectiv este comparat cu numărul de cazuri noi
raportate de reţeaua de epidemiologie la pct. 11 „Boli infecţioase şi
parazitare".
„Activitatea spitalului, sanatoriului, secţiei
(compartimentului), cabinetului de pneumologie"
Se completează anual de către fiecare dintre tipurile
de unităţi menţionate mai sus. Se trimite la ASPJ, care le trimite, la rândul
său, la Centrul Naţional pentru Organizarea şi Asigurarea Sistemului
Informaţional şi Informatic în Domeniul Sănătăţii Bucureşti.
DPF transmite lunar către CASJ lista nominală a
pacienţilor care intră în tratament antituberculos, iar lunar, trimestrial,
semestrial, la 9 luni şi anual, rapoarte care cuprind numeric cazurile aflate
în tratament, pe tipuri de regimuri terapeutice, numărul de investigaţii
bacteriologice şi radiologice efectuate, precum şi cheltuielile aferente acestora.
Anual, fiecare laborator judeţean transmite către LNR
situaţia examinărilor bacteriologice efectuate şi situaţia personalului din
laboratoarele respective, folosind pentru aceasta formulare standardizate.
RAŢIONALIZAREA REŢELEI DE SERVICII
Pentru asigurarea desfăşurării în condiţii optime a
activităţilor în cadrul PNCT se vor face evaluarea şi raţionalizarea resurselor
existente: infrastructură (clădiri), aparatură, personal.
ASIGURAREA INFRASTRUCTURII
Având în vedere starea actuală a clădirilor în care
funcţionează unităţile de pneumoftiziologie, este imperios necesară evaluarea
acestora din punctul de vedere al criteriilor standardelor europene pe care
trebuie să le îndeplinească în vederea acreditării acestora.
Se vor întreprinde demersuri
pentru întocmirea proiectelor necesare reabilitării şi refacerii circuitelor
funcţionale ale clădirilor, precum şi pentru accesarea de fonduri.
Această activitate va fi precedată de o evaluare a
necesarului în funcţie de:
- accesibilitatea şi adresabilitatea populaţiei la
servicii medicale;
- dimensionarea serviciilor în funcţie de nivelul
endemiei din teritoriul respectiv;
- restructurarea sistemului de asistenţă, în sensul
creşterii ponderii asistenţei medicale în ambulatoriu şi reducerii asistenţei
spitaliceşti;
- asigurarea disponibilităţii personalului medical, ca
număr şi nivel de competenţă;
- asigurarea măsurilor de control al transmiterii
infecţiilor. Raţionalizarea infrastructurii se referă la toate tipurile de unităţi de pneumoftiziologie: spitale,
secţii, ambulatorii, laboratoare bK.
Vechile unităţi de tip sanatorial vor fi restructurate
în sensul schimbării destinaţiei acestora: asistenţa bolnavilor cronici,
unităţi medico-sociale etc.
Aparatură de radiologie şi laborator de
bacteriologie
Se va avea în vedere faptul că aparatura existentă în
acest moment în reţeaua de pneumoftiziologie nu corespunde cu standardele
europene.
Laboratoare
Se va avea în vedere ca în perioada derulării PNCT 2007
- 2011 să fie asigurate condiţiile obţinerii acreditării tuturor laboratoarelor
de bacteriologie bK: infrastructură, aparatură etc.
Raţionalizarea reţelei de laboratoare bK se va face
după o prealabilă evaluare a acesteia.
Numărul de laboratoare necesar pentru asigurarea unui
diagnostic de calitate va fi stabilit în funcţie de criteriile recomandate
internaţional şi adaptate situaţiei specifice din România.
De asemenea, se va avea în vedere asigurarea
accesibilităţii unităţilor de pneumoftiziologie la serviciile de diagnostic
bacteriologic asigurate de către aceste laboratoare.
OMS organizează periodic misiuni de supervizare a
laboratoarelor de bacteriologie din România de către reprezentanţii
Laboratorului Supranaţional de Referinţă din Stockholm, urmate de recomandări
care sunt puse la dispoziţia conducerii MSP şi PNCT
ASIGURAREA SERVICIILOR DE ASISTENŢĂ MEDICALĂ ÎN
CADRUL PNCT
Având în vedere tendinţa de dezvoltare a sectorului
privat în domeniul asistenţei medicale, vor fi luate măsuri pentru asigurarea
funcţionării PNCT conform cu recomandările OMS pentru
un control eficient al TB.
Parteneriatul public-privat va fi încurajat pentru
ameliorarea calităţii serviciilor medicale din reţeaua de pneumoftiziologie.
Cabinetele de pneumologie vor fi subordonate metodologic
DPF.
Parteneriatul cu orice alte organizaţii guvernamentale şi neguvernamentale, cu societatea civilă etc.
va fi încurajat pentru maximizarea rezultatelor PNCT.
Asigurarea cu personal
Intregul personal încadrat în reţeaua de
pneumoftiziologie are obligaţia respectării prevederilor PNCT.
Va fi asigurată:
- teritorializarea epidemiologică a MF pentru
persoanele neasigurate;
- teritorializarea pe medici pneumologi;
- accesibilitatea la servicii de pneumoftiziologie: un
medic specialist la 50.000 de locuitori.
MONITORIZAREA Şl EVALUAREA PNCT
Una dintre componentele DOTS
este monitorizarea şi evaluarea activităţii PNCT. Pentru aceasta se utilizează
indicatori-cadru de măsurare a performanţelor subprogramului „Supravegherea şi
controlul tuberculozei" şi indicatori epidemiometrici care măsoară
impactul măsurilor luate prin PNCT (a se vedea anexa nr. 18, care face parte
integrantă din prezentele norme metodologice).
FINANŢAREA PNCT
Resursele financiare necesare finanţării PNCT provin de
la bugetul de stat, din veniturile proprii ale MSP şi din bugetul Fondului
naţional unic de asigurări sociale de sănătate.
ANEXA Nr. 1 la normele metodologice
FIŞA POSTULUI
coordonatorului DPF teritorial
Titlul postului: Coordonator
al DPF teritorial
Departamentul/Unitatea/Secţia: DPF teritorial
Descrierea postului
A. Sarcini/Responsabilităţi
• Organizează şi răspunde de întreaga activitate a DPF.
• Răspunde de implementarea măsurilor PNCT în
teritoriul arondat DPF.
• Examinează suspecţii de TB care se prezintă la DPF
din propria iniţiativă, trimişi de MF sau de alte eşaloane medicale, comunicând
ulterior acestora rezultatul.
• Asigură administrarea sub directă observare a
tratamentului antituberculos recomandat bolnavilor cu TB.
• Răspunde de înregistrarea corectă a bolnavilor în
Registrul de TB.
• Cunoaşte răspândirea infecţiei, grupele cu risc
epidemiologie în rândul populaţiei, indicatorii epidemiologici şi dinamica
teritorială a endemiei.
• Efectuează consultaţii medicale de specialitate
pentru angajare şi control medical periodic, cu sau fără contribuţie personală
a asiguratului.
• Efectuează îndrumarea metodologică a MF din
teritoriul arondat.
• Supervizează îndeplinirea atribuţiilor ce revin MF
conform PNCT.
• Efectuează comenzile lunare de medicamente pe care le
supune spre avizare CTJ al PNCT.
• Monitorizează şi evaluează
activităţile PNCT din teritoriu.
• Colectează, prelucrează şi raportează datele cuprinse
în sistemul informaţional al PNCT.
• Stabileşte incapacitatea de muncă şi emite
certificatul medical potrivit reglementărilor în vigoare.
• Urmăreşte şi asigură folosirea şi întreţinerea
corectă a mijloacelor din dotare.
• Colaborează cu alte instituţii din teritoriu, care au
responsabilităţi în realizarea PNCT (direcţia spitalului, CASJ, autorităţile
locale, organizaţii neguvernamentale cu activitate în
domeniu).
• Participă la acţiunile de informare şi instruire
organizate în cadrul judeţului de către unitatea judeţeană de evaluare şi
coordonare a PNCT.
B. Pregătire/Experienţă
Medic pneumolog specialist/primar
Relaţii cu alte posturi:
• de subordonare:
- se subordonează: CTJ al PNCT;
- are în subordonare: personalul angajat pentru
activităţile de control al TB în teritoriu;
• de colaborare cu:
- reprezentanţii ASPJ, CASJ, CMI, CAM, CERCM, CRR;
- medicii pneumologi din teritoriu;
- MF, asistenţa comunitară etc;
- medicii din alte specialităţi (din servicii
ambulatorii şi spitaliceşti);
- medicii din reţele paralele;
- medicii epidemiologi/epidemiologul-şef din ASPJ;
- reţeaua de învăţământ;
- autorităţile locale;
- organizaţii neguvernamentale, mass-media, poliţia
locală etc.
ANEXA Nr. 2a) la normele metodologice
REŢEAUA NAŢIONALĂ
de laboratoare pentru diagnosticul bacteriologic al
TB
Intre laboratoarele care
deservesc reţeaua clinică de pneumoftiziologie trebuie să fie o relaţie de
interdependenţă, de la nivelul de bază spre laboratoarele de referinţă şi
invers. Această interdependenţă defineşte de fapt „reţeaua naţională a
laboratoarelor de microbacteriologie", care se suprapune în linii mari
componentei clinice, ambele contribuind la realizarea obiectivelor PNCT,
desfăşurându-şi activitatea integrat în acest program.
Pentru buna funcţionare a reţelei este necesar să se
asigure supervizare de la nivelul imediat superior.
Asigurarea calităţii examinărilor bacteriologice este
posibilă prin cunoaşterea şi asumarea responsabilităţilor de către personalul
încadrat în aceste laboratoare, pe niveluri de activitate şi competenţă.
Laboratoarele judeţene sunt marcate cu bold.
|
LABORATORUL
NAŢIONAL DE REFERINŢĂ BUCUREŞTI
|
|
LRR SUD-EST
Buzău
|
LRR SUD
Colibaşi
|
LRR SUD-VEST Craiova
|
LRR
BUCUREŞTI - ILFOV
|
LRR VEST
Deva
|
LRR NORD-VEST Cluj-Napoca
|
LRR CENTRU
Braşov
|
LRR NORD-EST
Iaşi
|
|
BUZĂU
Buzău DPF III Spitalul Municipal Râmnicu
Sărat II
|
ARGEŞ
Spitalul de Pneumoftiziologie Leordeni
III
Penitenciarul Colibaşi III
Spitalul de Pneumoftiziologie Câmpulung II
Spitalul de Pneumoftiziologie Valea
Iaşului II Spitalul de Pneumoftiziologie Piteşti II
DPF Costeşti I
|
DOLJ
Spitalul de Pneumoftiziologie Leamna III
DPF Craiova II
DPF Calafat II DPFBechet II
DPF Filiasi II
DPF Băileşti I
|
INPNM LNR Bucureşti III
Sectoarele 1,2, 3,4
Laborator
M. Eminescu III
Laborator Spitalul
de Pneumoftiziologie
„Sfântul Ştefan" II
Spitalul de
Pneumoftiziologie
„V. Babeş" III
|
ARAD
Spitalul Clinic Municipal Arad III
Centrul de Sănătate Chişineu-Criş I
Spitalul Orăşenesc Lipova I
|
BIHOR Spitalul de Pneumoftiziologie
Oradea III
Spitalul Orăşenesc Marghita I
Spitalul Orăşenesc Salonta I
DPF Beiuş I
|
ALBA Spitalul Judeţean Alba Iulia II
Spitalul de Pneumoftiziologie Aiud II
Sanatoriul TB Câmpeni I
|
BACĂU Spitalul de Pneumoftiziologie Bacău III
Spitalul Penitenciar Târgu Ocna III
Spitalul Municipal Moineşti II
Spitalul Municipal Oneşti I
|
|
BRĂILA
Spitalul de Pneumoftiziologie Brăila III
|
DÂMBOVITA
DPF
Târgovişte III
Sanatoriul TB Moroieni II
DPF Găeşti I
|
GORJ
DPF
Târgu Jiu III
Spitalul de Pneumoftiziologie
Runcu-Dobriţa II
DPF Târgu Cărbuneşti I
|
Sectoarele 5, 6 II Secţia de cronici Alexandriei II Spitalul Militar Central III
Spitalul Militar de Urgenţă „Prof. dr.
Dimitrie Gerota" II
|
CARAS-
SEVERIN
Spitalul Judeţean
Reşiţa II
Spitalul Municipal
Caransebeş II
Spitalul Orăşenesc
Oraviţa-Marila I
|
BISTRITA-NĂSĂUD Spitalul Judeţean
Bistriţa II
|
BRAŞOV
Spitalul de Pneumoftiziologie Braşov III
|
BOTOŞANI
Spitalul de Pneumoftiziologie Botoşani
III
DPF Dorohoi II Sanatoriul Guranda I
|
|
CONSTANŢA Spitalul de
Pneumoftiziologie Constanţa III
Constanţa DPF II Spitalul de Pneumoftiziologie Agigea II
DPF Cernavodă I DPF
Hârşova I
DPF Mangalia I
DPF Medgidia I
|
PRAHOVA
Spitalul de Pneumoftiziologie Drajna III
DPF Ploieşti II Spitalul
Judeţean Ploieşti II
Spitalul de Pneumoftiziologie Floreşti II
|
MEHEDINŢI
Spitalul de Pneumoftiziologie
Drobeta-Turnu Severin III
DPF Orşova I
DPF Cujmir I
|
|
HUNEDOARA Spitalul Judeţean Deva III
Spitalul de Pneumoftiziologie Brad II
Spitalul de Pneumoftiziologie Geoagiu II
|
CLUJ
Spitalul Clinic de Pneumoftiziologie
Cluj-Napoca III Spitalul
Municipal Dej II
DPF Turda I
|
COVASNA
Spitalul Judeţean de Urgenţă Sfântu
Gheorghe II
|
IAŞI
Spitalul de Pneumoftiziologie Iaşi III
Spitalul Orăşenesc Paşcani II
|
|
GALAŢI
Spitalul de Pneumoftiziologie Galaţi III
|
IALOMIŢA
Spitalul Judeţean de Urgenţă Slobozia
III DPF Feteşti II
DPF Urziceni I
|
OLT
Spitalul Orăşenesc Scorniceşti III
Spitalul Municipal Slatina II
Spitalul Orăşenesc Corabia II
Spitalul Municipal Caracal II
DPF Drăgăneşti I
|
|
TIMIŞ
Spitalul Clinic „V. Babeş" III
Spitalul Municipal Lugoj II
Spitalul Orăşenesc Jimbolia II
|
MARAMUREŞ Spitalul de Pneumoftiziologie Baia Mare III
Spitalul Orăşenesc Sighetu Marmaţiei II Spitalul Orăşenesc Borşa I
Spitalul Orăşenesc Vişeu de Sus I
|
HARGHITA
Spitalul Judeţean Miercurea-Ciuc II
|
NEAMŢ
Centrul de excelenţă pentru MDR-TB
Bisericani III
Spitalul Judeţean Piatra-Neamţ II
DPF Roman I
DPF Târgu-Neamţ I
|
|
TULCEA
Tulcea III
Macin II
|
CĂLĂRAŞI
Spitalul de Pneumoftiziologie Călăraşi
III
DPF Călăraşi II
DPF Olteniţa II
DPF Budes'ti I
DPF Lehliu I
|
VÂLCEA
Spitalul de Pneumoftiziologie Mihăeşti
III
DPF Râmnicu Vâlcea II
DPF Horezu II
DPF Drăgăsani I
|
|
|
SATU MARE
Spitalul de Pneumoftiziologie Satu Mare
II
Spitaul Orăşenesc Bixad II
|
MUREŞ
Spitalul de
Pneumoftiziologie Târgu Mureş II
Spitalul Orăşenesc Târnăveni II
|
SUCEAVA Spitalul Judeţean Suceava II
Spitalul Orăşenesc Fălticeni II
Spitalul Orăşenesc Rădăuţi II
DPF Vatra Dornei I
DPF Câmpulung M. I
|
|
VRANCEA
Spitalul Judeţean Focşani III
|
GIURGIU
Spitalul de Pneumoftiziologie PNF Izvoru
III
DPF Giurgiu II
DPF Bolintin-Vale II
|
|
|
|
SĂLAJ
Spitalul Judeţean Zalău III
|
SIBIU
Spitalul de Pneumoftiziologie Sibiu III
Spitalul Municipal Mediaş II
|
VASLUI
Spitalul Judeţean Vaslui III
Spitalul Municipal Bârlad II
|
|
|
TELEORMAN
Spitalul de Pneumoftiziologie Roşiori de
Vede III DPF Videle I
|
|
|
|
|
|
|
ANEXA Nr. 2b) la normele metodologice
DPF DIN ROMÂNIA
pe euroregiuni şi pe judeţe
Unităţile care ţin de alte ministere, dar au rol de
DPF, sunt marcate cu litere italice.
|
DPF din
România
|
|
REGIUNEA SUD-EST
|
REGIUNEA SUD
|
REGIUNEA SUD-VEST
|
REGIUNEA
BUCUREŞTI-
ILFOV
|
REGIUNEA VEST
|
REGIUNEA NORD-VEST
|
REGIUNEA CENTRU
|
REGIUNEA NORD-EST
|
|
BUZĂU
Buzău
Râmnicu Sărat Nehoiu
Pogoanele
|
ARGEŞ
Piteşti
Câmpulung
Costeşti
Curtea de Argeş Topoloveni Penitenciarul Colibaşi
|
DOLJ
Craiova
Calafat
Bechet
Filiaşi
Băileşti
Segarcea
|
BUCUREŞTI Sectoarele 1,2,3, 4,5,6
Spitalul Militar Central
DPF din ambulatoriul Spitalului Militar
de Urgenţă „Prof. dr. Dimitrie Gerota"
|
ARAD
Arad
Chişineu-Criş
Ineu
Lipova
Sebiş
Pecica
|
BIHOR
Oradea
Marghita
Alejd
Beiuş
Salonta
|
ALBA
Alba Iulia
Câmpeni
Blaj
Cugir
Ocna Mureş
Sebeş
Aiud
|
BACĂU
Bacău
Moineşti
Oneşti
Buhuşi
Comăneşti
Penitenciarul
Târgu Ocna
|
|
BRĂILA
Brăila
Făurei
|
DÂMBOVIŢA
Târgovişte
Găeşti
Titu
Pucioasa
Moreni
Răcari
|
GORJ
Târgu Jiu
Târgu Cărbuneşti Motru
Novaci
|
ILFOV
Buftea
Baloteşti
Penitenciarul
Jilava
|
CARAŞ-SEVERIN
Reşiţa
Caransebeş
Oraviţa
Oţelu Roşu
Bocşa
Moldova Nouă
|
BISTRIŢA-NĂSĂUD Bistriţa Năsăud
|
BRAŞOV
Braşov
Făgăraş
Săcele
Rupea
Zămeşti
|
BOTOŞANI
Botoşani
Dorohoi
|
|
CONSTANTA
Constanţa DAT
Cernavodă
Hârşova
Mangalia
Medgidia
Băneasa
|
PRAHOVA
Ploieşti
Câmpina
Vălenii de Munte-
Drajna
Mizil
Sinaia
|
MEHEDINŢI Drobeta-Turnu
Severin
Orşova
Cujmir
Strehaia
Baia de Aramă
Vânju Mare
|
|
HUNEDOARA
Deva
Vulcan
Petroşani
Hunedoara
Brad
Haţeg
Orăstie
Ilia
|
CLUJ
Cluj-Napoca
Dej
Turda
Câmpia Turzii
Gherla
Huedin
|
COVASNA Sfântu Gheorghe Târgu Secuiesc
|
IAŞI
Iaşi
Paşcani
Târgu Frumos
Hârlau
|
|
GALAŢI
Galaţi I
Galaţi II
Târgu Bujor
Tecuci
|
IALOMIŢA
Slobozia
Feteşti
Urziceni
|
OLT
Slatina
Scomiceşti
Corabia
Caracal
Drăgănesti
Bals
|
|
TIMIŞ
Timişoara
Lugoj
Jimbolia
Făget
Deta
Sânnicolau Mare
|
MARAMUREŞ
Baia Mare
Sighetu Marmaţiei Borşa
Vişeu de Sus
Târgu Lăpuş
|
HARGHITA
Miercurea-Ciuc
Odorheiu
Secuiesc
Gheorgheni
Cristuru Secuiesc
Topliţa
|
NEAMŢ Piatra-Neamţ
Roman
Târgu-Neamţ
|
|
TULCEA Tul cea Macin Babadag
|
CĂLĂRAŞI
Călăraşi
Olteniţa
Budeşti
Lehliu
|
VÂLCEA
Râmnicu Vâlcea Horezu
Drăgăşani
Bălceşti
|
|
|
SATU MARE Satu Mare Cărei Negreşti
Tăşnad
|
MUREŞ
Târgu Mureş
Tâmăveni
Sighişoara
Reghin
Luduş
|
SUCEAVA
Suceava
Fălticeni
Rădăuţi
Vatra Dornei Câmpulung Moldovenesc
Gura Humorului
|
|
VRANCEA
Focşani
Adjud
Panciu
Vidra
|
GIURGIU
Giurgiu
Bolintin-Vale
Ghimpaţi
Mogoşeşti
|
|
|
|
SĂLAJ
Zalău
Jibou
Şimleu Silvaniei
|
SIBIU
Sibiu
Mediaş
|
VASLUI
Vaslui
Bârlad
Negreşti
Huşi
|
|
|
TELEORMAN
Roşiori de Vede
Videle
Turnu Măgurele
Zimnicea
Alexandria
|
|
|
|
|
|
|
ANEXA Nr. 2c) la normele metodologice
SITUAŢIA
spitalelor şi secţiilor de pneumoftiziologie în
România pe euroregiuni şi pe judeţe
|
Unităţile
cu paturi de pneumoftiziologie din România
|
|
REGIUNEA SUD-EST
|
REGIUNEA SUD
|
REGIUNEA SUD-VEST
|
REGIUNEA
BUCUREŞTI-
ILFOV
|
REGIUNEA VEST
|
REGIUNEA NORD-VEST
|
REGIUNEA CENTRU
|
REGIUNEA NORD-EST
|
|
BUZĂU
Secţia de pneumoftiziologie a Spitalului
Judeţean Buzău
Secţia de pneumoftiziologie a Spitalului
Municipal Râmnicu Sărat
|
ARGEŞ
Spitalul de
Pneumoftiziologie
Leordeni
Spitalul de
Pneumoftiziologie
Piteşti
Spitalul de
Pneumoftiziologie
Câmpulung
Spitalul de
Pneumoftiziologie
Valea Iaşului
Secţia de
pneumoftiziologie a Spitalului
Penitenciar
Colibaşi
|
DOLJ
Spitalul de Pneumoftiziologie Leamna
Clinica de pneumoftiziologie în Spitalul
Clinic nr. 3 „V. Babeş"
Craiova Spitalul de Pneumoftiziologie Poiana Mare
|
BUCUREŞTI
IMPMN cu Centrul de excelentă MDR-TB
Bucureşti Spitalul de Pneumoftiziologie „Sfântul Ştefan" cu Secţia de
pneumoftiziologie nr. 3: Cronici, Şos. Alexandriei
Secţia de pneumoftiziologie a Spitalului
Clinic „V Babeş"
Secţia de pneumoftiziologie a Spitalului
Militar Central
Secţia de pneumoftiziologie a Spitalului
Militar de Urgenţă „Prof. dr. Dimitrie Gerota"
|
ARAD
Secţia de
pneumoftiziologie
a Spitalului Clinic
Municipal Arad
Secţia de
pneumoftiziologie
a Spitalului
Orăşenesc Lipova
Secţia de
pneumoftiziologie
a Centrului de
Sănătate Chişineu- Criş
Secţia de
pneumoftiziologie
a Spitalului de
Boli Cronice Sebiş
Sanatoriul TB Bulei
Secţie a Spitalului
Clinic Municipal
Arad
|
BIHOR
Spitalul de Pneumoftiziologie Oradea
Secţia de pneumoftiziologie a Spitalului
Orăşenesc Marghita
Secţia de pneumoftiziologie a Spitalului
Orăşenesc Alejd
Secţia de TB Psihici a Spitalului de Psihiatrie Nucet
|
ALBA
Spitalul de Pneumoftiziologie Aiud
Sanatoriul TB Câmpeni
|
BACĂU
Spitalul de
Pneumoftiziologie
Bacău
Secţia de
pneumoftiziologie
a Spitalului
Orăşenesc Moineşti
Secţia de
pneumoftiziologie a Spitalului
Penitenciar Târgu Ocna
|
|
BRAILA
Spitalul de Pneumoftiziologie Brăila
|
DÂMBOVIŢA
Sanatoriul TB
Moroieni
Secţia de
pneumoftiziologie a Spitalului Orăşenesc
„Mănăstirea Dealului"
Târgovişte
|
GORJ
Spitalul de Pneumoftiziologie
Runcu-Dobriţa
|
ILFOV
Secţia de pneumoftiziologie a Spitalului Penitenciar Jilava
|
CARAŞ-SEVERIN Secţia de
pneumoftiziologie a Spitalului Judeţean Reşiţa
Secţia de pneumoftiziologie a Spitalului
Municipal Caransebeş
Secţia de pneumoftiziologie
„Marila" a Spitalului Orăşenesc Oraviţa Secţia de pneumoftiziologie a
Spitalului Orăşenesc Moldova Nouă
|
BISTRIŢA-NĂSĂUD Secţia de
pneumoftiziologie a Spitalului Judeţean Bistriţa
|
BRAŞOV
Spitalul de Pneumoftiziologie Braşov
|
BOTOŞANI
Spitalul de Pneumoftiziologie Botoşani
Sanatoriul TB Guranda
|
|
CONSTANŢA Spitalul de Pneumoftiziologie
Constanţa cu Secţie Militară Constanţa Spitalul de Pneumoftiziologie Agigea
|
PRAHOVA
Spitalul de Pneumoftiziologie Drajna
Spitalul de Pneumoftiziologie Breaza
Secţia de pneumoftiziologie a
Spitalului Judeţean Ploieşti
Spitalul de Pneumoftiziologie Floreşti
|
MEHEDINŢI
Spitalul de Pneumoftiziologie
Drobeta-Turnu
Seve rin
|
|
HUNEDOARA Sanatoriul TB Brad
Sanatoriul TB Geoagiu
Secţia de
pneumoftiziologie a Spitalului Municipal
Hunedoara
Secţia de pneumoftiziologie a Spitalului
Judeţean Deva
Secţia de
pneumoftiziologie a Spitalului Municipal Vulcan
|
CLUJ
Spitalul Clinic de
Pneumoftiziologie
„Leon Daniello"
Cluj-Napoca
Secţia de
pneumoftiziologie
a Spitalului
Municipal Dej
Sanatoriul TB
Săvădisla
|
COVASNA
Secţia de pneumoftiziologie a Spitalului
Judeţean Sfântu Gheorghe
|
IAŞI
Spitalul Clinic de
Pneumoftiziologie
Iaşi
Preventoriul TB
Deleni
|
|
GALAŢI
Spitalul de Pneumoftiziologie Galaţi
|
IALOMIŢA
|
OLT
Spitalul de Pneumoftiziologie Scomiceşti
Secţia de pneumoftiziologie a Spitalului
Municipal Caracal
|
|
TIMIŞ
Secţia de pneumoftiziologie a Spitalului Clinic „V Babeş" Timişoara Secţia de
pneumoftiziologie copii a Spitalului „L. Ţurcanu" Timişoara Secţia de
pneumoftiziologie a Spitalului Municipal Lugoj
Secţia de pneumoftiziologie a Spitalului
Orăşenesc Jimbolia
Secţia de pneumoftiziologie a Spitalului
Orăşenesc Făget
|
MARAMUREŞ Spitalul de Pneumoftiziologie
Baia Mare
Secţia de pneumoftiziologie a Spitalului
Orăşenesc Sighetu Marmatiei Secţia de pneumoftiziologie a Spitalului
Orăşenesc Vişeu de Sus
|
HARGHITA
Secţia de pneumoftiziologie a Spitalului
Judeţean Miercurea-Ciuc
|
NEAMŢ
Centrul de excelenţă MDR-TB Bisericani
|
|
TULCEA
Secţia de pneumoftiziologie a Spitalului
Judeţean Tulcea
|
CĂLĂRAŞI
Spitalul de
Pneumoftiziologie
Călăraşi
Compartimentul de
pneumoftiziologie al Spitalului Orăşenesc
Budeşti
Compartimentul de
pneumoftiziologie al Spitalului Municipal Olteniţa
|
VÂLCEA
Spitalul de Pneumoftiziologie Mihăeşti
|
|
|
SATU MARE
Spitalul de Pneumoftiziologie Satu Mare
Secţia de pneumoftiziologie a Spitalului
Orăşenesc Bixad
|
MUREŞ
Spitalul de Pneumoftiziologie Târgu
Mureş
Secţia de pneumoftiziologie a Spitalului
Orăşenesc Sighişoara
|
SUCEAVA
Secţia de pneumoftiziologie a Spitalului
Judeţean Suceava
Spitalul de Pneumoftiziologie Fălticeni
Spitalul de Pneumoftiziologie Rădăuţi
|
|
VRANCEA
Secţia de pneumoftiziologie a Spitalului
Judeţean Focşani
|
GIURGIU
Spitalul de Pneumoftiziologie Izvoru
|
|
|
|
SĂLAJ
Secţia de pneumoftiziologie a Spitalului
Judeţean Zalău
Secţia de pneumoftiziologie a Spitalului
Jibou
Secţia de pneumoftiziologie a Spitalului
Şimleu
Silvaniei
|
SIBIU
Spitalul de Pneumoftiziologie Sibiu
Secţia de pneumoftiziologie a Spitalului
Municipal Mediaş
|
VASLUI
Secţia de pneumoftiziologie a Spitalului
Judeţean Vaslui
Secţia de pneumoftiziologie a Spitalului
Municipal Bârlad
Secţia de pneumoftiziologie a Spitalului
Orăşenesc Negreşti
|
|
|
TELEORMAN
Spitalul de Pneumoftiziologie Roşiori de
Vede
|
|
|
|
|
|
|
ANEXA Nr. 3a) la normele metodologice
FIŞA POSTULUI
CTJ al PNCT
Titlul postului: Manager
judeţean al PNCT
Departamentul/Unitatea/Secţia:
Descrierea postului
A. Sarcini/Responsabilităţi
• Analizează nevoile şi serviciile de sănătate
specifice, precum şi resursele disponibile (personal, aparatură, instrumentar,
materiale, consumabile, întreţinere etc).
• Stabileşte priorităţile pentru Programul judeţean de control al TB.
• Elaborează proiectul judeţean pentru Programul
judeţean de control al TB (obiective specifice, plan de implementare, resurse
umane, materiale, financiare) şi îl propune spre avizare.
• Coordonează şi răspunde de implementarea la nivel
judeţean/de sector.
• Colaborează cu alte instituţii cu responsabilităţi în
realizarea Programului judeţean de control al TB (ASPJ, CASJ, autorităţi
locale, organizaţii neguvernamentale cu activitate în domeniu etc).
• Organizează activitatea de îndrumare metodologică a
TB în teritoriu (inclusiv vizite de îndrumare în teritoriu).
• Organizează, supraveghează şi răspunde de colectarea
datelor (inclusiv cele referitoare la activitatea laboratoarelor bK), stocarea
informaţiilor, prelucrarea şi raportarea acestora.
• Analizează periodic datele colectate (lunar,
trimestrial, anual) si identifică problemele specifice pe care le comunică UCM.
• Răspunde de întocmirea Registrului judeţean de TB.
• Evaluează eficacitatea şi eficienţa măsurilor
Programului judeţean de control al TB şi realizează acţiuni de corecţie
necesare.
• Coordonează, controlează şi avizează comenzile lunare
de medicamente la nivelul unităţii de profil din judeţ.
• Organizează, coordonează şi răspunde de Programul
judeţean de educaţie continuă şi instruire a medicilor de familie, asistenţilor
comunitari şi altor categorii de personal în ceea ce priveşte activităţile de
control al TB.
• Colaborează cu ASJP pentru realizarea programelor de
promovare a sănătăţii şi educaţie pentru sănătate în domeniu.
• Participă la acţiunile de informare şi instruire
privind PNCT la nivelul UCM.
• Propune şi participă la alocarea fondurilor către
unităţile implementatoare, din toate sursele de finanţare ale PNCT la nivelul
judeţului.
• Monitorizează şi evaluează activităţile PNCT la
nivelul judeţului.
B. Pregătire/Experienţă:
- medic pneumolog specialist/primar;
- aptitudini manageriale, cursuri de management sanitar,
management de proiecte;
- autoritate profesională în domeniul medical.
C. Performanţa
aşteptată:
- elaborarea până la data de 31 iulie a fiecărui an a
propunerii de proiect judeţean pentru Programul judeţean de control al TB
(obiective specifice, plan de implementare, resurse umane, materiale şi
financiare necesare) şi înaintarea spre avizare de către UCM;
- realizarea planului de îndrumare metodologică (orarul
vizitelor, rapoarte de vizită);
- actualizarea continuă a registrului judeţean;
- încadrarea în termenele stabilite a raportărilor şi
comenzilor de medicamente;
- realizarea planului de
formare şi instruire tehnică a MF, asistenţilor comunitari şi altor categorii
de personal;
- realizarea monitorizării activităţilor din Programul
judeţean de control al TB;
- evaluarea periodică a Programului judeţean de control
al TB şi realizarea raportului anual.
D. Solicitări
speciale pentru post
- noţiuni de operare calculator;
- capacitate de interpretare şi analiză a datelor
colectate;
- abilităţi de comunicare şi muncă în echipă.
Relaţii cu alte posturi
• de subordonare:
- se subordonează CTN;
- are în subordonare:
- personalul angajat pentru implementarea Programului
judeţean de control al TB;
• de colaborare cu:
1. CPAIC a MSP;
2. reprezentanţii ASJP, CASJ, CMI, CAM, CERCM, CRR;
3. medicii pneumologi din teritoriu;
4. MF, asistenţa comunitară etc;
5. medicii din alte specialităţi (din servicii
ambulatorii şi spitaliceşti);
6. medicii din reţele paralele;
7. medicii epidemiologi/epidemiologul-şef din ASPJ;
8. Direcţia sanitară de statistică;
9. reţeaua de învăţământ;
10. autorităţile locale;
11. organizaţii neguvernamentale;
12. mass-media;
13. poliţia locală.
ANEXA Nr. 3b) la normele metodologice
FIŞA POSTULUI
coordonatorului laboratorului bK
Relaţii ierarhice:
- se subordonează atât managerului organizaţiei din
care face parte, cât şi coordonatorului laboratorului bK ierarhic superior.
Coordonatorul laboratorului bK judeţean şi al LNR se mai subordonează CTJ şi,
respectiv, CTN.
Responsabilităţi specifice (în funcţie de nivelul
laboratorului):
- participă şi supervizează activitatea specifică de
diagnostic bacteriologic al TB: examenul microscopic, cultura şi antibiograma
bK, identificarea tulpinilor din complexul MT;
- supervizează completarea corectă a documentelor,
registru de laborator, formulare de solicitare a examenului bK;
- semnează buletinele de analiză;
- se preocupă de procurarea materialelor şi reactivilor
specifici laboratorului;
- se preocupă de menţinerea în funcţiune a
echipamentelor;
- participă la programarea, monitorizarea şi evaluarea
activităţilor PNCT la nivel local;
- estimează necesarul de materiale şi aparatură, în
vederea stabilirii planului de achiziţii şi investiţii;
- participă la efectuarea şi supervizarea controlului
intern şi extern de calitate al examenului microscopic, al antibiogramei şi al
culturii;
- participă la actualizarea şi distribuirea ghidurilor
cu tehnici de diagnostic bacteriologic al TB şi a ghidurilor privind
organizarea şi managementul laboratoarelor de microbacteriologie;
- asigură evaluarea anuală a performanţelor
profesionale individuale ale personalului în raport cu exigenţele posturilor;
- se preocupă de perfecţionarea cunoştinţelor teoretice
şi practice ale personalului mediu din subordine; ţine evidenţa formării şi
perfecţionării personalului din laborator;
- analizează datele ce reflectă activitatea
laboratoarelor arondate şi propune măsuri de îmbunătăţire a activităţii;
- participă activ la acţiuni de îndrumare şi control al
activităţilor din teritoriu şi din ţară în domeniul microbacteriologiei;
- iniţiază şi participă la proiecte de cercetare
locale, naţionale sau internaţionale care implică activitatea de diagnostic al
TB;
- întocmeşte date statistice referitoare la activitatea
laboratorului şi le transmite laboratorului bK judeţean şi CTJ.
Responsabilităţi generale:
- respectă regulamentul de
ordine interioară;
- respectă confidenţialitatea tuturor aspectelor legate
de locul de muncă, indiferent de natura acestora;
- respectă normele PSI;
- respectă normele de protecţie a muncii;
- respectă circuitele funcţionale din laborator;
- respectă programul de muncă;
- respectă codul de etică şi deontologie profesională;
- îndeplineşte orice alte sarcini stabilite de forul
ierarhic superior;
- răspunde disciplinar, civil şi material pentru toate
pagubele provocate unităţii prin executarea defectuoasă a atribuţiilor sau prin
neexecutarea acestora;
- coordonează, controlează şi răspunde de aplicarea
Ordinului ministrului sănătăţii şi familiei nr. 219/2002 pentru aprobarea
Normelor tehnice privind gestionarea deşeurilor rezultate din activităţile
medicale şi a Metodologiei de culegere a datelor pentru baza naţională de date
privind deşeurile rezultate din activităţile medicale, cu modificările şi completările
ulterioare;
- împreună cu tot personalul laboratorului participă la
aplicarea cerinţelor standardului SR-EN 17025/2005 în vederea acreditării
laboratorului şi a menţinerii calităţii pentru laboratoarul acreditat.
ANEXA Nr. 4*) la normele metodologice
Cod :
Unitatea care solicita____________________________
Medic solicitant (parafa)_________________________
FORMULAR PENTRU SOLICITARE / RAPORTARE
EXAMEN BACTERIOLOGIC PENTRU TUBERCULOZĂ
Nume pacient______________________________________
CNP |__|__|__|__|__|__|__|__|__|__|__|__|__|
Adresa______________________Data
naşterii __/__/__/ Sex M |__| F |__|
Cod pacient/Fişa nr.________________________
FO/Nr. registru
consultaţii______________________________________
Recoltat de __________________________La data __ /__ /
Nr. identificare produs_____________________
Examenul solicitat M |__| C |__| ABG: HR |__|; extinsă |__|
Scop examen Diagnostic /Monitorizare |__| respectiv T
|__|
Categoria de bolnav Caz Nou/Recidiva/Eşec/
Abandon/Transfer/Cronic |__| Alt produs decât
sputa___________
ORGANIZAŢIA.................................................. LABORATORUL
.....................................................
Adresa :.................................................................
Telefon/Fax/e-mail:.....................................................
Aspectul sputei:
sero-mucoasa (M)|__| |__| |__|
muco-purulentă (P)|__| |__| |__| hemoptoică (H)|__| |__| |__| salivă (S) |__| |__| |__|
REZULTATE MICROSCOPIE (EXPRIMARE SEMICANTITATIVĂ)
Data primirii probei __/__/__
Nr. Reg. Laborator...........................
Data eliberării rezultatului __/__/__
Semnătura de primire rezultat.............................
|
Specimen
|
Rezultat
|
Pozitiv (grade) BAAR
|
|
|
|
3+
|
2+
|
1 +
|
1-9
|
|
A
|
|
|__|
|
|__|
|
|__|
|
|__|
|
|
B
|
|
|__|
|
|__|
|
|__|
|
|__|
|
|
C
|
|
|__|
|
|__|
|
|__|
|
|__|
|
Procedura aplicată: Direct |__|
Centrifugare |__| Coloraţie Z-N |__| Fluorescentă |__|
Nu se prelucrează |__| Motivul...............................(se trece nr, specimenului
în cauză)
Efectuat.......................................Verificat.......................................
Validat (şef
laborator)......................................................................
(Semnătura şi parafa)
(Semnătura şi parata)
*) Anexa nr. 4 este reprodusă în facsimil.
REZULTATE CULTURA ( EXPRIMARE SEMICANTITATIVĂ)
Data primirii probei ___/___/_____
Nr. Reg. Laborator..........................
Data eliberării rezultatului __/__/_____
Semnătura de primire
rezultat...........................
|
Specimen
|
Rezultat
|
Pozitiv (grade)
|
|
|
|
3+
|
2+
|
1 +
|
1-30col
|
|
A
|
|
|__|
|
|__|
|
|__|
|
|__|
|
|
B
|
|
|__|
|
|__|
|
|__|
|
|__|
|
|
C
|
|
|__|
|
|__|
|
|__|
|
|__|
|
Identificare ; complex tuberculosis |__| alte
micobacterii |__|...................
Procedura aplicata: Cu picătura |__| Centrifugare |__|
Nu se prelucrează |__|
Motivul..................................................................(se
trece nr. specimenului în cauză)
Efectuat.......................................Verificat..................................Validat
(şef
laborator)...............................................
(Semnătura şi parafa)
(Semnătura şi parata)
Rezultatul se referă mimai la produsul examinat.
Acest document poate fi reprodus numai cu acordul
laboratorului emitent şi numai integral.
AUTOCOPIATIVE: în 3 exemplare:
- originalul se va returna solicitantului cu rezultatul
microscopiei;
- prima copie se va returna solicitantului cu rezultatul
culturii;
- a doua copie se va păstra în arhiva laboratorului
timp de cel puţin 2 ani.
Notă: Fiecare filă a formularului de solicitare conţine
instrucţiuni de completare a fiecărei rubrici.
ANEXA Nr. 5 la normele metodologice
RECOLTAREA PRODUSELOR BIOLOGICE
Investigaţia bacteriologică are o poziţie centrală atât
în diagnosticul şi monitorizarea cazurilor de TB, cât şi în evaluarea PNCT, de
aceea toate etapele acesteia - de la pregătirea pacientului şi recoltarea
produsului patologic până la citirea şi interpretarea rezultatelor - trebuie
tratate cu deosebită atenţie.
Aspecte generale
Calitatea produselor patologice este esenţială pentru
obţinerea unor rezultate de încredere. In acest sens trebuie să se ţină seama
de următoarele:
1. Recoltarea şi manipularea produselor patologice se
fac astfel încât:
- să se evite contaminarea cu bacterii şi fungi a
produsului patologic;
- să se evite diseminarea germenilor în mediul ambiant;
- să se evite infectarea
personalului medical implicat.
2. Recoltarea şi manipularea produselor patologice se
fac sub supravegherea unui cadru medical instruit privind reducerea riscului de
contaminare a produselor, care trebuie să se asigure că s-a recoltat un produs
provenit din focarul lezional, de la un pacient corect identificat şi în
cantitate suficientă pentru prelucrare în laborator.
3. Respectarea normelor generale de recoltare, şi
anume:
• în cazul persoanelor suspecte de TB, produsele se
recoltează înainte de începerea tratamentului
antituberculos;
• în cazul bolnavilor aflaţi sub tratament, se
recoltează produse patologice numai după întreruperea tratamentului timp de 3
zile;
• repetarea examenului bacteriologic în zile succesive
(la suspecţii de TB pulmonară se pot recolta până la 9 spute, în cazul în care
primele examinări au fost negative, iar suspiciunea de TB se menţine);
• caracteristicile recipientelor pentru recoltarea
sputei:
- confecţionate din material plastic, incasabil,
transparent - pentru a observa cantitatea şi calitatea produsului patologic
fără a deschide recipientul;
- cu deschidere largă (minimum 35 mm diametru) - pentru
evitarea contaminării pereţilor exteriori ai recipientului;
- capacitate de 30-50 ml pentru spută şi adaptată pentru fiecare tip de produs patologic;
- cu capac cu filet care închide etanş recipientul;
- cu posibilitatea de a fi marcate cu uşurinţă.
Recoltarea sputei spontan expectorate, în sectorul clinic.
Primul pas pentru un diagnostic fiabil este obţinerea
unor produse de calitate.
Recoltarea sputei:
• se efectuează ori de câte ori se suspectează
diagnosticul de TB pulmonară;
• se efectuează în spaţii special destinate, acolo
unde acestea există;
• se face după instruirea prealabilă a bolnavului
privind tehnica;
• se face sub supravegherea unui cadru medical
(geam/vizor la boxa de recoltare);
• se respectă măsurile de control al infecţiilor şi
condiţiile optime de păstrare a produselor patologice: ventilaţie
corespunzătoare (fereastră), lămpi U.V., măşti, frigider pentru păstrarea
probelor (până la maximum 4 zile), uşă cu geam pentru supravegherea recoltării.
Pacientul trebuie instruit înaintea recoltării cu
privire la etapele acesteia:
• clătirea gurii cu apă pentru îndepărtarea
resturilor alimentare;
• efectuarea a două inspiraţii
profunde urmate de reţinerea respiraţiei după fiecare dintre ele timp de câteva
secunde, apoi o a treia inspiraţie profundă, urmată de un expir forţat. Se
declanşează tuşea care va uşura expectoraţia;
• depunerea sputei în recipientul/flaconul
care se ţine lipit de buze;
• verificarea de către cadrul mediu a calităţii sputei:
3-5 ml spută cu particule purulente. Dacă aceasta nu corespunde, se repetă
manevra de recoltare;
• fixarea strânsă a capacului prin înfiletare;
• spălarea pe mâini cu apă şi săpun;
• se recoltează 3 probe pentru fiecare control
bacteriologic: două sub supraveghere medicală şi una din prima spută emisă
spontan dimineaţa.
In cazul persoanelor care nu tuşesc şi nu expectorează
spontan sau care înghit expectoraţia (de exemplu, femeile) se vor aplica
tehnici speciale de provocare şi recoltare a sputei:
• aerosoli expectoranţi cu soluţie de NaCl 10%;
• lavajul laringo-traheal cu ser fiziologic steril;
• tubajul gastric folosind sonde Nelaton sau Einhorn;
• aspiratul bronşicsau lavajul
bronho-alveolar prin bronhoscopie. Trimiterea probelor la laborator se face
astfel:
• împreună cu formularul de solicitare standardizat,
completat la toate rubricile - un singur formular pentru toate cele 3 probe, cu
date de identificare identice pe recipient şi pe formular;
• etichetarea flacoanelor se face cu numele şi
prenumele bolnavului pe corpul recipientului, nu pe capac;
• de către persoana desemnată de medicul de laborator,
în cutii speciale din plastic, prevăzute cu despărţituri pentru separarea şi
fixarea flacoanelor cu spută;
• imediat după recoltare sau, dacă nu este posibil,
acestea se păstrează la frigider (4°C), maximum 3-4 zile (pentru a minimaliza
multiplicarea florei de asociaţie).
Factorii care pot influenţa viabilitatea micobacteriilor
trebuie cunoscuţi pentru a fi evitaţi, şi anume:
• administrarea de antibiotice cu efect antituberculos:
- Rifampicină, Streptomicină;
- Kanamicină, Amikacină;
- Ciprofloxacină, Ofloxacină;
- Claritromicină, Amoxicilină + Acid clavulanic;
• conservarea în formol sau recoltarea pe EDTA;
• contactul prelungit cu sucul gastric (peste 3-4 ore);
• păstrarea probelor la căldură sau lumină;
• întârzierea prelucrării produselor patologice (peste
5 zile);
• congelarea prelevatelor.
ANEXA Nr. 6 la normele
metodologice
TEHNICA TESTĂRII TUBERCULINICE
Materiale necesare efectuării testului tuberculinic
(metoda Mantoux) sunt:
• produsul biologic - tuberculina (se verifică
valabilitatea şi calitatea produsului biologic);
• seringă etanşă de unică folosinţă de 1 ml divizată în
0,10 ml, prevăzută cu ac special pentru injecţii intradermice (de 10 mm, cu
bizou scurt);
• soluţie dezinfectantă - alcool de 75%;
• vată.
Locul inoculării: de preferat, faţa anterioară a
antebraţului stâng, treimea medie, în tegument sănătos.
Tehnica administrării trebuie să fie foarte riguroasă,
după cum urmează:
• verificarea valabilităţii şi calităţii produsului
biologic;
• dezinfectarea tegumentului cu alcool sanitar;
• întinderea pielii de pe faţa ventrală a antebraţului
pentru a facilita introducerea strict intradermică a tuberculinei;
• se injectează intradermic 0,1 ml PPD care realizează
de obicei o papulă ischemică de 5-6 mm cu aspect de „coajă de portocală";
aceasta nu trebuie tamponată după ce s-a extras acul.
IDR corectă este confirmată de
lipsa sângerării şi de obţinerea papulei.
Citirea testului este cantitativă.
Citirea rezultatului se face între 48 şi 72 de ore
(ideal la 72 ore) de la administrare, când induraţia este maximă şi reacţia
nespecifică dispare.
Se măsoară diametrul transversal al zonei de induraţie
(nu al eritemului) cu ajutorul unei rigle transparente. Eventual se marchează
limitele, după ce au fost palpate şi delimitate exact punctele extreme ale
diametrului transversal. Se recomandă ca citirea să nu se facă după 72 de ore, întrucât se subestimează
rezultatul.
Interpretarea calitativă (tipurile Palmer) nu mai este
de actualitate.
Vaccinarea BCG induce în mod obişnuit pentru 3-4 ani o
reacţie care de obicei nu depăşeşte 10 mm. O reacţie mai intensă traduce foarte
probabil infecţia naturală cu MT
Citirea şi interpretarea trebuie făcute de personal cu
experienţă, care notează mărimea diametrului induraţiei şi data citirii.
Interpretarea testului
Reacţia pozitivă: se
consideră reacţie pozitivă o reacţie inflamatorie/induraţie de peste 10 mm la
locul inoculării, care apare până la 72 de ore de la injectare. Induraţia este
reliefată, eritematoasă, delimitată net de restul tegumentului normal.
O reacţie pozitivă semnifică numai infecţia cu MT (dar
şi cu M. bovis -
natural sau vaccinai) şi nu poate fi argument pentru TB boală. O reacţie
intensă locală nu semnifică obligatoriu prezenţa bolii, însă sugerează mai
degrabă o infecţie cu MT decât o reacţie încrucişată cu alte micobacterii sau
cu vaccinarea BCG.
Convenţional se admite că:
• reacţia sub 9 mm semnifică alergie postvaccinală BCG
(în primii ani după naştere) sau infecţie cu micobacterii atipice;
• reacţia moderată, 10-14 mm, sugerează infecţia cu MT;
• reacţia intensă, peste 15 mm (hiperergia), cu/fără ulceraţii,
flictene, nu semnifică neapărat TB activă, ci doar probabilitatea unui risc
crescut de evolutivitate a leziunilor.
Reacţia (intens) pozitivă la PPD este marker al
infecţiei TB, nu certifică TB activă.
Dacă rezultatul testului a fost pozitiv, repetarea
lui nu mai furnizează informaţii suplimentare şi nu este indicată!
Virajul tuberculinic constă
în pozitivarea unei testări care succedă uneia cu rezultat negativ şi, dacă nu
este consecinţa unei vaccinări BCG, traduce o infecţie de dată recentă.
Reacţia negativă (anergia)
reprezintă lipsa de răspuns la injectarea ID a tuberculinei şi poate fi
întâlnită în mai multe situaţii:
• organismul testat este neinfectat;
• organismul este infectat şi se află în faza
antealergică;
• organismul este infectat, dar testul este efectuat după o boală anergizantă;
• stingerea hipersensibilităţii după tratament sau
spontan, In cazul în care rezultatul la 2 UI PPD IC65
este negativ, dar există suspiciunea infecţiei (copil
aflat în contact strâns cu o sursă de TB activă), se poate
repeta imediat testul cu 10 UI PPD IC65 în
antebraţul opus, după aceeaşi tehnică, sau la un interval de 6-8 săptămâni, cu
2 UI PPD, pentru a verifica menţinerea negativităţii.
Reacţiile fals-negative pot
fi determinate de:
• factori individuali;
• factori legaţi de produsul
utilizat:
- inactivarea produsului prin: expunere la lumină şi
căldură, diluţii improprii, denaturări biochimice, contaminare, adsorbtie
parţială pe pereţii fiolei;
• factori umani:
- tehnică defectuoasă de administrare: prea puţin
produs, tamponarea energică după injectare, sângerare;
- erori de citire.
O reacţie negativă
la PPD sugerează o afecţiune netuberculoasă, dar nu exclude
diagnosticul de TB.
Reacţiile fals-pozitive pot
fi cauzate de:
• tehnica sau citirea defectuoasă
(interpretarea reacţiilor nespecifice, injectarea subcutană a tuberculinei);
• alte infecţii micobacteriene atipice;
• vaccinare BCG;
• reacţii încrucişate cu alţi antigeni bacterieni (de
exemplu, ASLO în cantitate mare).
Incidente, accidente
Testul nu este însoţit de
incidente şi accidente grave. Se citează frecvent edemul marcat şi inflamaţia
produsă de introducerea subcutană a tuberculinei.
Pentru detalii, vezi Ghidul de diagnostic şi tratament
al TB la copil.
Se va avea în vedere extinderea unor metode noi pentru diagnosticul infecţiei tuberculoase latente,
pe măsură ce acestea vor deveni disponibile, bazate pe producţia de interferon
gama a limfocitului activat de TB (IGRA), precum şi PCR.
ANEXA Nr. 7*) la
normele metodologice
FISA PENTRU ANCHETA EPIDEMIOLOGICA
Data primirii fisei de anunţare ___/___/______
Data anunţarrii medicului epidemiolog ___/___/______
Data anunţării medicului de familie ___/___/______
Dala declanşarii anchetei epidemiologice __/__/______
Anehota epidemiologica
Nume........................................ Prenume
............................................. Cod pacient...............
CNP.......................................Sex ........ Data naşterii __/__/______B.I....................................
Locul naşterii (localitatea / judeţul / ţara)
.....................................................................................
Cetăţenia...........................................Naţionalitatea....................................................................
Adresa
reala.....................................................Telefon
.............................................................
Adresa legala.............................................................................................................................
Ocupaţia.....................................Locul de
munca......................................................................
Categoria sociala............................Asigurat.......
Medic de familie.............................................
Nr. registru TB____Data declarării___/__/____Categoria caz la înregistrare
Anul primei înregistrări______ Anul ultimei
înregistrări______
Localizarea TB Diagnostic principal.............................................................................................
Diagnostice secundare
...............................................................................................................
Examen bacteriologic iniţial:
M....................C..................
ABG: sensibilitate ..............................................rezistenţă.....................MDR...........................
Examen
histopatologic:...............................................................................................................
Condiţii
asociate:....................................................................Istoric
detenţie..............................
Cicatrice BCG (la copiii 0-15 ani):.........mm
Internat la spitalul...............................judeţul...................din
data __/__/______
Data începerii traiamenlului: __/__/______
Regimul __ Asocierea_________Ritmul _/7
Sursa de imbolnavire:
identificata da / nu...............................
Numele si prenumele sursei:..............................
Codul de pacient al sursei:
...............................
Locuinta: nr. camere___Nr.
persoane în locuinţa___din care copii___
Alte observaţii:....................................................................................................
Contacţii intradomiciliari
* Adulţi
Mume Prenume Dala naşterii Ex.
efectuat Data Rezultatul
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
* Copii.
Nume Prenume Data
naşterii Ex. efectuat Data Rezultatul
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
Contractii extradomociliari:
Nume Prenume Data naşterii Ex.
efectuat Data Rezultatul
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
Masuri luate:
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
_______________________________________________________________
Menţiuni speciale:
Data încheierii anchetei epidemiologice;
*) Anexa nr. 7 este reprodusă în facsimil.
ANEXA Nr. 8 la normele metodologice
DEFINIŢIA CAZULUI DE TB
Cazul de TB este:
• bolnavul cu TB confirmată bacteriologic sau
histopatologic (HP); sau
• bolnavul care nu are confirmare,
dar referitor la care medicul pneumolog are suficiente date clinice şi
paraclinice pentru a decide începerea tratamentului antituberculos.
Orice tratament antituberculos trebuie instituit numai
de către un medic pneumolog sau cu avizul medicului pneumolog al teritoriului
de care aparţine unitatea în care este instituit tratamentul.
Cazul de TB este definit în funcţie de localizarea
bolii, confirmarea bacteriologică sau histopatologică şi istoricul terapeutic.
I. Localizarea TB poate fi:
• pulmonară - dacă leziunile sunt în parenchimul
pulmonar, în arborele traheo-bronşic sau în laringe. Acestea sunt forme
contagioase, importante din punct de vedere epidemiologie;
• extrapulmonara - dacă leziunile sunt în alte locuri
decât cele de mai sus.
In situaţia în care pacientul are o singură localizare
a bolii, aceasta va fi înscrisă la diagnostic principal şi va determina
încadrarea cazului în una dintre categoriile de mai sus.
Cazul de TB cu două sau mai multe localizări, dintre
care cel puţin una pulmonară, va avea ca diagnostic principal pe cel al
localizării pulmonare, iar ca diagnostic secundar (diagnostice secundare) pe
cel (cele) al (ale) localizărilor extrapulmonare. Cazul se va înregistra ca TB
pulmonară.
Dacă niciuna dintre localizări nu este pulmonară, se va
considera diagnostic principal cel al localizării celei mai grave, iar
celelalte localizări vor fi înscrise ca diagnostice secundare. Cazul se va
înregistra ca TB extrapulmonara.
TB diseminată, dacă are şi localizare pulmonară, se va
considera cu localizare pulmonară. Se va înscrie la diagnostic principal forma
anatomo-radiologică pulmonară, iar la diagnostice secundare localizările
extrapulmonare. In absenţa determinării pulmonare, se va înregistra ca TB
extrapulmonara, se va considera diagnostic principal diagnosticul formei celei
mai grave, iar diagnostice secundare, cele ale celorlalte determinări.
TB copilului va fi considerată cu localizare pulmonară
dacă se evidenţiază leziuni ale parenchimului pulmonar, ale arborelui
traheo-bronşic sau ale laringelui (diagnostic principal), respectiv cu
localizare extrapulmonara dacă nu sunt leziuni în aceste structuri (diagnostic
principal, cel al localizării unice sau cel al localizării celei mai grave).
Adenopatia traheo-bronşică, neînsoţită de alte determinări, va fi înregistrată
ca diagnostic principal, iar localizarea se va considera extrapulmonara. Dacă
însă la un astfel de caz rezultatul examenului bacteriologic din spută sau dintr-un
alt produs recoltat este pozitiv, se va presupune existenţa fistulei
traheo-bronşice, chiar dacă aceasta nu a fost evidenţiată, iar cazul va fi
înregistrat cu localizare pulmonară.
II. Confirmarea
bacteriologică sau histopatologică (definiţiile ECDC)
Un control bacteriologic pentru diagnostic înseamnă
examinarea a minimum 3 eşantioane de produs patologic, iar pentru monitorizarea
evoluţiei sub tratament, a cel puţin două.
Dată fiind importanţa examenului bateriologic, se
impune necesitatea obţinerii unor produse patologice cât mai de calitate (în
cazul sputei, prin instruirea prealabilă a pacientului şi prin utilizarea de
mijloace de provocare a expectoraţiei, când este cazul).
Conform definiţiilor ECDC pot exista 3 tipuri de caz de
TB, în funcţie de confirmarea diagnosticului în laborator:
1. cazul de TB confirmat:
- pozitiv la cultură (C+) -
este cel care are cel puţin o cultură pozitivă din sputa recoltată înainte de
începerea tratamentului antituberculos, indiferent de rezultatul microscopiei;
- pozitiv la microscopie (M+) + detecţia acizilor
nucleici în produsul patologic + criterii clinice
pentru TB.
Cazul de TB pulmonară pozitiv la microscopie (M+) este
cel care are la examenul eşantioanelor de spută recoltate înainte de începerea
tratamentului pentru TB:
• cel puţin două rezultate M(+);
• un rezultat M(+) şi unul C(+);
• un rezultat M(+) şi aspect radiologie interpretat de
specialist ca sugestiv de TB pulmonară activă;
2. cazul de TB probabil este pacientul care are cel puţin una dintre confirmările de laborator
de mai jos:
• este pozitiv la microscopie (M+);
• au fost detectaţi acizi
nucleici pentru MT în produsul patologic;
• are un examen histopatologic pozitiv pentru TB.
Pentru toţi pacienţii suspectaţi de TB extrapulmonara
se vor recolta specimene specifice în funcţie de localizare, pentru a fi
examinate atât histopatologic, cât şi bacteriologic.
Din orice biopsie recoltată de la un pacient suspect de
TB trebuie să se facă şi un examen bacteriologic pentru MT (bK);
3. cazul de TB posibil este
pacientul cu TB pulmonară sau extrapulmonara care nu are niciunul dintre
criteriile de confirmare de mai sus, dar care este considerat de medicul
pneumolog ca fiind un caz de TB activă şi la care acesta decide instituirea
tratamentului antituberculos.
III. Istoricul terapeutic
Inregistrarea unui pacient se va face conform istoricului său terapeutic real.
1. Cazul nou (N) este
pacientul care nu a luat niciodată tratament cu medicamente antituberculoase în
asociere pe o perioadă mai mare de o lună de zile.
Chimioprofilaxia TB efectuată cu un singur medicament
sau cu două (de exemplu, copii, infectaţi cu HIV) nu se consideră tratament
antituberculos.
2. Cazul cu retratament este unul din următoarele categorii:
• Recidivă (R) - pacientul care a fost evaluat ca „Vindecat" sau „Tratament
complet" în urma unui tratament antituberculos
anterior şi care are un nou episod de TB confirmată.
Cazurile de TB neconfirmate pot fi de asemenea
înregistrate ca retratamente pentru „Recidivă", dar astfel de situaţii
trebuie să fie rare şi bine argumentate prin examene clinice şi investigaţii
paraclinice;
• Retratament pentru eşec
(E) - pacientul care începe un retratament după ce
a fost evaluat ca „Eşec" al unui tratament anterior;
• Retratament pentru abandon (A) - pacientul care începe un retratament după ce a fost evaluat ca
„Abandon" al unui tratament anterior şi este bacteriologic pozitiv sau la
care medicul pneumolog decide reluarea unui nou tratament după abandonul celui
anterior;
• Cronic (C) -
pacientul care începe un nou retratament după ce a fost evaluat ca „Eşec"
al unui retratament.
ANEXA Nr. 9 la normele metodologice
ANUNŢAREA, ÎNREGISTRAREA SI DECLARAREA
CAZURILOR
Anunţarea
Orice caz de TB (confirmat bacteriologic sau
histopatologic ori în cazul căruia medicul pneumolog decide începerea
tratamentului antituberculos) va fi anunţat de către medicul care a
diagnosticat cazul sau care a iniţiat tratamentul, în 48 de ore, prin Fişa de
anunţare a cazului de tuberculoză*), la DPF pe al cărui teritoriu bolnavul are
adresa stabilă (locuieşte în fapt, conform declaraţiei sale), indiferent de
adresa sa legală (înscrisă în documentele de identitate).
Bolnavul cu TB fără locuinţă va fi anunţat la DPF de
care aparţine zona în care acesta declară că îşi duce existenţa.
Pentru a furniza DPF toate informaţiile de care acesta
are nevoie pentru înregistrarea şi declararea cazului, ca şi pentru declanşarea
AE, în fişa de anunţare se vor completa toate rubricile cât mai corect. Se vor
menţiona pe foaia de observaţie a bolnavului data completării şi cea a
trimiterii fişei de anunţare.
DPF va verifica, prin
personalul propriu sau prin MF, dacă pacientul locuieşte în fapt la adresa
înscrisă în fişa de anunţare.
Inregistrarea şi declararea
Dacă bolnavul locuieşte la adresa dată, va fi
înregistrat în Registrul de tuberculoză*) al DPF şi în baza de date
electronică, după o prealabilă verificare în baza de date naţională pentru a se
evita dubla raportare. Datele înscrise vor corespunde episodului de îmbolnăvire
care este înregistrat.
In acelaşi timp, medicul pneumolog din DPF va informa,
prin scrisoare medicală*), medicul epidemiolog al teritoriului respectiv şi MF
la care este înscris pacientul despre existenţa cazului (focarului) de TB
pentru declanşarea AE. In situaţia în care pacientul nu este înscris pe listele
unui MF, scrisoarea medicală va fi trimisă MF căruia îi este arondat
epidemiologie teritoriul în care locuieşte bolnavul.
Dacă se constată că pacientul nu locuieşte la adresa
înscrisă în fişa de anunţare, aceasta va fi returnată unităţii care a trimis-o,
cu menţiunea „Pacientul nu locuieşte la adresa indicată".
In situaţia în care pacientul a fost externat şi nu se
mai prezintă la DPF care a primit anunţarea, acesta va înregistra şi va declara
cazul, va face investigaţii pentru găsirea lui şi, dacă nu îl va găsi într-un
interval de 12 luni de la înregistrare, îl va evalua ca „Pierdut". Dacă
bolnavul apare în acest interval la DPF, fie va continua tratamentul (dacă va
locui în continuare la adresa la care a fost înregistrat), fie se va opera
transferul la un alt DPF, în teritoriul căruia declară că s-a mutat.
Atât în Registrul de tuberculoză al DPF, cât şi în baza
de date electronică vor fi înregistrate toate cazurile de TB, indiferent dacă sunt cazuri noi, retratamente pentru
diverse situaţii sau transferuri din alte DPF, în ordinea cronologică a
apariţiei lor.
Pentru fiecare caz de TB înregistrat din soft se
tipăreşte automat Fişa de declarare a cazului de tuberculoză*).
Fiecare caz de TB înregistrat va fi obligatoriu şi
evaluat atunci când există toate informaţiile necesare evaluării, dar nu mai
târziu de 12 luni de la data declarării.
Dacă după 12 luni de la declarare pacientul este încă
în tratament, el va fi evaluat ca „Continuă tratamentul" (C) şi va fi
imediat înregistrat din nou în Registrul de tuberculoză, în categoria
„Continuare de tratament" (K). In următoarele 12-24 luni, după ce va
încheia tratamentul şi va avea toate rezultatele controalelor bacteriologice, i
se va stabili o categorie de evaluare finală.
Infirmarea
Dacă după înregistrare se constată că diagnosticul de
TB activă nu a fost corect stabilit, cazul respectiv va fi infirmat, dar numai
de către medicul pneumolog din DPF în evidenţa căruia se află pacientul.
Stabilirea noului diagnostic care face obiectul
infirmării într-o altă unitate decât DPF va fi anunţată DPF prin Fişa de
anunţare a infirmării diagnosticului de tuberculoză în spital*).
Infirmarea (I) se poate opera
numai între momentul declarării şi cel al evaluării, iar după înscrierea sa
atât în Registrul de tuberculoză, cât şi în bazele de date electronice va fi
echivalentă cu o categorie de evaluare finală.
Decesul unui bolnav de TB în spital
In cazul decesului unui bolnav de TB în spital, după
anunţarea cazului la DPF de care acesta aparţine, decesul va fi de asemenea
semnalat DPF - în 24 de ore - prin Fişa de anunţare a decesului pacientului cu
tuberculoză în spital*), pentru a fi operat în evidenţele TB ale unităţii.
Transferul
De asemenea, dacă un caz îşi schimbă adresa după
înregistrare până la momentul evaluării, se va opera electronic transferul,
conform Formularului pentru transferul bolnavilor*), iar după primirea
confirmării preluării bolnavului de cel de-al doilea DPF, se va înscrie în
Registrul de tuberculoză, la rubrica „Evaluare", „Mutat" (M) şi se va
trimite documentaţia medicală. DPF care primeşte pacientul îl va înregistra în
Registrul său de tuberculoză, cu categoria „Transferat" (T).
Dacă cel de-al doilea DPF nu confirmă primirea şi
pacientul nu apare la noua adresă în maximum două luni de la anunţarea
transferului, primul DPF va evalua cazul ca „Pierdut" (P).
*) Formularele sunt reproduse în facsimil.
|
Spitalul.........................................
Judeţul.....
Către
Dispensarul PF....................................................
Judeţul.....................................................
FIŞA DE ANUNŢARE A CAZULUI DE
TUBERCULOZĂ
Nume..............................
Prenume........................Cod
pacient.....................................
CNP ................................. Sex M |__| F |__| Data naşterii (zz/ll/aaaa).......................
Localitatea/Judetul/Tara naşterii
.....................................................................................
Domiciliul
real................................................................................................................
Domiciliul legal...............................................................................................................
Asigurat Da |__| NU |__| Medic de
familie........................Adresa MF..........................
Data internarii (zz/ll/aaaa)..........Categorie caz N |__| R |__|
E |__| A |__| C |__|
Localizare **P |__| E |__|
Diagnostic principal TB
...............................................................................................
Diagnostice secundare
TB............................................................................................
Boli
asociate................................................................................................................
Examen
histopatologic.................................................................................................
Examen bacterie logic la internare: Produsul
patologic.......................................
|
Data intrării produsului in
laborator
|
Laboratorul
|
Nr. registru laborator
|
Rezultat
microscopie
|
Rezultat
cultura
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Antibiograma;
sensibilitate..........................................rezistenţa...........................................
Data începerii tratamentului actual
(zz/ll/aaaa).......................................................................
Regimul terapeutic: 1 |__| 2|__| 3|__| Individualizat |__|
medicamente/doze (mg)...................
ritm de administrare: .../7
Anunţai post-mortem |__| Data decesului (zz/ll/aaaa).......
Data completarii ............................, MEDIC
(semnătura şi parafa)...................................
*N-caz nou;R=recidiva;F=retratament dupa esec;A= retratament dupa
abandon; C = cronic.
**P = pulmonara; E = extrapulmonara
|
|
Dispensarul de pneumoftiziologie ...............................
Judeţul................................
Către Dl / Dna
Dr...............................................
Specialitatea............................................
Adresa.....................................................
SCRISOARE MEDICALĂ
Stimate coleg.
Vă informăm că pacientul (nume.
prenume)..........................................................................
cu
CNP.........................................................de
sex.................născut la data de............. în
localitatea...................................................judeţul............................................ domiciliat in localitatea.................................judeţul
(sectorul)....................
str.........................................
nr..........bl.........sc.......et.........ap.......... a fost diagnosticat cu: Tuberculoza pulmonară |__| extrapulmonara |__|
BK
microscopie................. cultură.......................
In consecinţă, vă rugăm să declanşaţi ancheta epidemioiogica
pentru acest caz de tuberculoză şi să ţineţi legătura cu medicul
pneumofliziolog teritorial pentru a primi informaţii suplimentare.
Vă mulţumim,
Data Medic
pneumoftiziotog (semnătura şi parafa)
.............................
............................................................................
|
|
Spitalul.........................................
Judeţul..................................
Catre Dispensarul
PF..................................
Judeţul.............................................
FIŞA DE ANUNŢARE A INFIRMARII
DIAGNOSTICULUI DE TUBERCULOZĂ IN SPITAL*
Nume..............................
Prenume........................Cod
pacient...........................................
CNP ................................. Sex M |__| F |__| Data naşterii (zz/ll/aaaa)............................
Domiclilul
real......................................................................................................................
Data Internării (zz/ll/aaaa)........Categorie caz** N |__| R |__| E |__| A |__| C |__| Localizare*"P |__| E|__|
Diagnostic principal
TB.......................................................................................................
Diagnostice secundare
TB...................................................................................................
Examen hisropatologic.........................................................................................................
Examen bacleriotogic la Internare: produsul
patologic...........................................................
Rezultat microscopie............................. Rezultat
cultură.......................................................
Antibiograma: sensibilitate...........................rezistenţa..........................................................,
Data începerii tratamentului actual (zz/ll/aaaa)........................................................................
Regimul terapeutic: 1 |__| 2 |__| 3 |__| individualizata
Data trimiterii fişei de anunţare a cazului................................................................................
Diagnostic final..................................................................................................................
Motivele
infirmării.................................................................................................................
Data completării........................... MEDIC (semnătura şi parata)........................................
*Se completează de către medicul die spital în cazul in carer un pacient cu tuberculoză anunţat
antrior este infirmal in cursul internarii
**N = caz nou ; R=recidiva. E = retratament dupa esec; A=
ratratamant dupa abandon: C = cronic.
***P = pulmonara; E = extrapulmonara.,
|
|
Spitalul.........................................
Judeţul.........................................
Catre Dispensarul
PF.................................
Judeţul............................................
FIŞA DE ANUNŢARE A DECESULUI
PACIENTULUI CU TUBERCULOZĂ ÎN
SPITAL*
Nume...................................................
Prenume........................Cod pacient.....................
CNP ........................................ Sex M |__| F |__| Data naşterii (zz/ll/aaaa)....................,
Domiciliul real......................................................................................................................
Data internării (zz/ll/aaaa).........Categorie caz**N |__| R |__| E |__| A |__| C |__| Localizare***P |__| E |__|
Diagnostic principal TB........................................................................................................
Diagnostice secundare
TB....................................................................................................
Boii asociate........................................................................................................................
Examen
histopatologic..........................................................................................................
Examen bacteriologic la internare: produsul
patologic............................................................
Rezultat microscopie.................................... Rezultat cultură................................................
Antibiograma: sensibilitate........................................rezistenţa...............................................
Data începerii tratamentului actual
(zz/ll/aaaa)........................................................................
Regimul terapeutic: 1 |__| 2 |__| 3 |__| individualizat o
Data trimiterii fişai de anunţare a cazului...............................................................................
Data decesului.........................
Cauza decesului TB |__| altă cauză |__|
Date completării ............................... MEDIC (semnătura şi parafa)..................................
*Se completează de către medicul din spital to cazul in cere un
pacient cu tuberculoze anunţat anterior decedează in cursul internării.
**N = caz nou: R = recidiva: E = retratament după eşec; A =
retratament după abandon: C = cronic. ***P = pulmonară: E = extrapulmonara.
|
|
Judetul:
Disp. Pneumoftiziologice…………………………………..
Fişa de declarare a cazului de
tuberculoza
...........................................
Cod pacient...............................................
Nume.
prenume..................................................................................................................
CNP.:...................................................Sex:......................
Data nasterii .............................
Judet nastere...............................................Loc
nastere:......................................................
Cetatenie:.........................................................Varsta.........................................................
Adresa: Judet:..................................................................
Localitate ...............................
Strada...........................................Nr......................Bl:..................Sc..................................
Et.:.......................................
Ap.:......................................
Mediu:..................................
Categoria
sociala..................................................Ocupatie:............................................
Anul primei declarări:..........................................................................
Anul ultimei declarari.........................................................................
Data declarare:...................................Nr. registru
dispensar..............................................
Categeorie
caz..................................Localizare:...............................................................
Diagnostic
principal............................................................................................
Diagnostice secundare
:....................................................................................
Examen bacteriologic la deplasare: Data
:...............................
Microscopie : ..................
Cultura: ...........................
Antibiograma:...................
MDR:............................................
Examen histopatologic ................
Condiţii asociate
:....................................................................................................
Internat: Data internarii
.................................................
Spital/Sanatoriu:
.............................................
Tratament: Data inceperii:...............................................
Asociere
.....................................................
Ritm:............................................................
Data completarii .......................................... Medic:........................................
(semnatura si parafa)
|
|
Formular pentru transferul
bolnavilor
De la
dispensarul.....................................Judet:....................................................................
La dispensarul:
.......................................Judet....................................................................
Cod pacient:.........................
Nume.
prenume...................................................................................................................
CNP:..........................................Sex:.....................................
Data nasterii:.........................
Judet nastere:
..................................................................Loc.
nastere :................................
Adresa anterioara: ...............................................................................................................
Judet:.......................................................................Localitate:............................................
Strada ..............................................Nr
..................Bl............................... Sc....................
Et.:.............................Ap...........................................Mediu:..............................................
Data doctorare:.....................Nr. registru
disp..:.......................Categorie caz:.......................
Diagnostic............................................................................................................................
Examen bacteriologic la deplasare :
Data:........................................
Microscopie.............................
Cultura.....................................
Antibiograma.........................................................
MDR................................................................
Examen bistopatologic: .....................................
Tratament: Data inceperii: ...............................
Asociere:......................................
Data......................
Medic:..............................................
( semnatura si parafa)
............................................................................................................................................
La dispensarul ...........................................Judet
:................................................................
Da la dispensarul:.......................................Judeţ:.................................................................
Cod pacient:............................
Nume.
prenume...................................................................................................................
C.N.P.:........................................Sex..............................
Data nasterii ...............................
Tara/judet nastere:........................................Loc.
nastere :..................................................
Adresa actuala:...................................................................................................................
Judet.......................................................................Localitate.............................................Strada:........................................
Nr.:...............................Bl.:...........................Sc.:...........
Et.........................Ap.:..............................Mediu:..............................................
Data inregistrarii in registrul de tuberculoza ......................................
Nr. registru disp.....................
Data:..................................
Medic:........................................
(semnatura si parafa)
(Returnati acesta parte a formularului la dispensarul de la care a
venit pacientul)
|
SPITAL/DISPENSAR TB.........................................................
JUDEŢ........................................................................................
CĂTRE: DISPENSARUL
TB...................................................
CENTRUL
MDR.......................................................................
Coordonatorul Tehnic
Judeţean................................................
FIŞA DE ANUNŢARE A CAZULUI DE TUBERCULOZĂ MDR*)
NUME................................................PRENUME....................Cod
pacient/Fisa nr...................
Nr reg.
Consultaţii.....CNP/CE/PASS |__|__|__|__|__|__|__|__|__|__|__|__|__|__|__|__|__|__|
Localitate/Judet/Tara naşterii.......................................................................................................
Domiciliul
real.............................................................................................................................
Domiciliul legal............................................................................................................................
Asigurat DA/NU Medic de
familie..................................Adresa cab.
MF...........................
FO............Data internării
(z/l/an) / / Categorie caz: N R E A C.......Localizare:
pulm/extrap
Diagnostic principal
TB..............................................................................................................
Diagnostice secundare TB..........................................................................................................
Boli
asociate...............................................................Ex
liistopatologic......................................
Ex. bacteriologic: laboratorul.................................................Produs
patologic............................
|
Microscopie
|
Cultura
|
ABC
|
|
Data intrării prod. in lab
|
Nr. in
reg. Lab
|
Rez./data eliberării
|
Data intrării prod. in lab
|
Nr. in
reg. Lab
|
Rez./data eliberării
|
Data intrării prod. in lab.
|
Nr. in
reg. Lab
|
Rez./data eliberării
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
REZISTENTA : H /R /Z/ E/ S/ K/A/ Ptm/ Cs/ Q/ CM/PAS (se marchează si alte rezistente asociate )
Declară că a mai făcut tratament anti-TB anterior:
DA/NU Anul |__| |__| |__| |__|
|__| |__| |__| |__|
|__| |__| |__| |__|
Anunţat post-mortem |__|
Data decesului (z/l/an)...................................
Data completării......................... MEDIC
(semnătura şi parafa)........................
*) Formularul este reprodus în facsimil.
ANEXA Nr. 10*) la normele metodologice
Cod pacient
FIŞA DE TRATAMENT A TUBERCULOZEI
|
Nume si prenume..............................................
CNP.....................Sex M/F Varsta ................
Adresa reală ....................................................
Diagnosticul......................................................
|
|
Dinspensarul TB ...............................................
Judeţul..............................................................
Medicul de familie. ...........................................
Adresa MF.......................................................
|
|
Localizare
|__| Pulmonara
|__| Exlrapulmonara
|
|
|__| Caz nou |__| Recidiva
|__| Transfer |__| Esec
|__| Abandon |__| Cronic
|
|
Regim standard1 1 |__| 2 |__| 3 |__| individualizat2
|__| Modificat pentru......... Data ........../.............
Faza iniţială4 |__| |__| |__| |__| |__| Ritm: |__| |__| Semnătura şi parafa.............................................
H R Z E S 7/7
3/7
Faza de continuare |__| |__| |__| |__| |__| Ritm: |__| |__| Semnătura şi parafa...................................
Regim individualizat
Data .... /.../........... Asocierea5 |__| |__| |__|
|__| |__| |__| Ritmul .../7 Semnătura şi
parafa.................
Dozele
..../..../..../..../..../..../
Data.... /.../.......... Asocierea |__| |__| |__| |__| |__| |__|
Ritmul .../7 Semnătura si parafa..................
Dozele
..../..../..../..../..../..../
Data ..../.../.......... Asocierea |__| |__| |__| |__| |__| |__|
Ritmul .../7 Semnătura si
parafa...................
Dozele
.../..../..../..../..../..../
|
|
|
Data
|
Nr. laborator
|
Microscopia
|
Cultura
|
ABG
|
|
TO
|
|
|
|
|
|
|
T2
|
|
|
|
|
|
|
T3
|
|
|
|
|
|
|
T4-T5
|
|
|
|
|
|
|
T6-TB
|
|
|
|
|
|
|
Evaluare: V|__| T |__| D |__| E |__| A |__| P |__| C |__|
Data
evaluarii.........................................................................
|
|
Anul
...............
Ziua
|
|
Luna
|
1
|
2
|
3
|
4
|
5
|
5
|
7
|
8
|
9
|
10
|
11
|
12
|
13
|
14
|
15
|
16
|
17
|
18
|
19
|
20
|
21
|
22
|
23
|
24
|
25
|
26
|
27
|
28
|
29
|
30
|
31
|
Semnătura pacientului
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Se va nota cu ,X" in dreptul zilei in care s-a
administrat medicaţie striet
supravegheată, „A" în cazul medicatiei autoadministrate şi „-"în cazul in care s-a omis priza. 1,2,3,4,5,6 Vezi verso.
1)Regim standard 1 =
2HRZE(S) + 4HR3
2 = 2HRZES + 1HRZE +
5HRE3
3 = 2HRZ + 4HR3
2) Regim individualizai = regim care includă si medicamenta anituberculoase de linia a
doua (in afară de HRZES).
3) Se precizezza
cauza modificării regimului:
chimiorezistenta, reactii adverse, alele.
4) Se va scne doza in
mg pentru fiecare medicament
5) Simbolurile utilizata pentru medicamentele antituberculoase sunt;
H: Isoniazidă; R: Rifampicină; Z: Pireazinamidă: E:
Etambutol; S: Streptomicină; K: Kanamicina; Ak:
Amikacina.; Cpx: Ciprofioxacina; Ofx: Ofloxacina: Ptm:
Protionamidă;
Etm: Etionamida: Cs: Cicloserina; Cpm: Capreomocina;
Pas: Acid paraaminosalicilic; Cl: Claritomicina.
6) Semnătura
pacientului pentru confirmarea primirii rnadicamentelor pe luna respectiva.
*) Anexa nr. 10 este reprodusă în facsimil.
ANEXA Nr. 11 la normele metodologice
REACŢIILE ADVERSE ŞI
INTERACŢIUNEA CUALTE MEDICAMENTE
Reacţii adverse la medicamentele antituberculoase de
linia I
|
Efecte adverse
|
Medicamente responsabile
|
Atitudine
|
|
Minore
|
|
Se continuă tratamentul, se verifică dozele.
|
|
anorexie, greaţă, dureri abdominale
|
Z, R
|
Se va efectua controlul funcţiei
hepatice.
Se administrează tratamentul cu un prânz sau la culcare.
|
|
dureri articulare
|
Z
|
Aspirina
|
|
senzaţia de arsură la nivelul membrelor inferioare
|
H
|
Piridoxina 100 mg/zi
|
|
colorarea în portocaliu a urinei
|
R
|
Se asigură pacientul că este un fenomen
normal.
|
|
Efecte adverse
|
Medicamente responsabile
|
Atitudine
|
|
Majore
|
|
Se întrerupe medicamentul responsabil.
|
|
prurit, erupţie cutanată, peteşii
|
S, H, R, Z
|
• dacă nu este intens şi nu influenţează calitatea vieţii, se va
trata cu antihistaminice
• dacă este generalizat, se opreşte medicamentul responsabil şi
se reintroduc după remisiune la 2-3 zile, în ordinea R, H, E şi Z
• în cazul apariţiei rasului peteşial, se face controlul
trombocitelor; dacă trombocitele sunt scăzute, se întrerupe R
|
|
surditate (fără dop de ceară)
|
S
|
Se întrerupe S, se foloseşte E.
|
|
vertij sau nistagmus
|
S
|
Se întrerupe S, se foloseşte E.
|
|
icter, hepatită (excluderea altor cauze)
|
H, Z, R
|
Hepatita medicamentoasă este atestată de creşterea AST de 3 ori
în cazul asocierii simptomelor clinice (sindrom dispeptic, icter) sau când
AST creşte de 5 ori la pacientul asimptomatic. Se întrerupe medicamentul
cauzator şi se utilizează medicamente cu hepatotoxicitate mică.
|
|
confuzie (suspiciune de insuficienţă hepatică acută)
|
majoritatea medicamentelor anti TB
|
Se întrerupe tratamentul, se investighează funcţia hepatică şi
protrombina.
|
|
alterarea acuităţii vizuale
|
E
|
Se întrerupe E.
|
|
şoc, purpură, IRA
|
R
|
Se întrerupe R.
|
Reacţiile adverse se consemnează obligatoriu pe fişa de
farmacovigilenta care se trimite la Agenţia Naţională a Medicamentului.
Toate informaţiile menţionate mai sus se găsesc
sintetic în „Fişa de tratament al tuberculozei" (anexa nr. 10).
Interacţiunea cu alte medicamente
Foarte rar diferitele medicamente asociate terapiei cu
antituberculoase modifică concentraţia medicatiei anti
TB.
Influenţa medicamentelor antituberculoase asupra
concentraţiei serice a altor medicamente
|
Medicamentul
|
Interacţiunea medicamentoasă
|
|
Izoniazida
|
• influenţează metabolizarea unor anticonvulsivante: fenitoină,
carbamazepină
• creşte activitatea toxică a acetaminofenului, teofilinei
• creşte concentraţia serică a diazepamului
|
|
Rifampicina
|
• scade activitatea unor antibiotice (doxiciclină,
cloramfenicol), levotiroxinei
• reduce concentraţia serică a corticosteroizilor,
benzodiazepinelor, fenitoinei, digoxinei, nifedipinei, propanololului,
endoprilului, teofilinei
• scade eficacitatea anticoncepţionalelor orale
• poate interacţiona cu unele medicamente antiretrovirale,
compromiţând atât tratamentul anti TB, cât şi pe cel antiretroviral
|
ANEXA Nr. 12*) la normele metodologice
(Sursa: Indrumarul de supraveghere epidemiologică a tuberculozei şi de monitorizare a
aplicării PNCT", paginile 18- 19)
FIŞA DE TRATAMENT PENTRU CAZUL CU MDR TB
Pacientul:
Nume.........................................Prenume...........................................
Categorie pacient1) N |__| R |__| E |__| A |__| C |__|
|
Tratament medicamentos:
|
Data
|
H
|
R
|
E
|
Z
|
S
|
K
|
Ak
|
Cpm
|
Q
|
Ca
|
Ptm
|
PAS
|
Cl
|
|
|
Debut tratament individualizat
Modificari ale schemei de tratament
|
/ /
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
/ /
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
/ /
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
/ /
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
/ /
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
/ /
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
/ /
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Incheiere tratament
|
/ /
|
Evaluare finală a cazulului2:V
|__| T |__| E |__| A |__| D |__| M |__| P |__|
|
|
Tratament chirurgical:
Data: Tipul:
|
|
Reacţii adverse:
|
|
Data
|
Medicam.
suspectat
|
Tipul reacţiei adversa
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Luna
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
11
|
12
|
13
|
14
|
15
|
16
|
17
|
18
|
19
|
20
|
21
|
22
|
23
|
24
|
25
|
26
|
27
|
28
|
29
|
30
|
31
|
Ade- renta
|
Ex. direct
|
Cultura
|
Rezis-tente
ABG
|
|
Zi
|
|
1
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
9
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
11
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
12
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
13
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
14
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
15
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
16
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
17
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
18
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
19
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
20
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
21
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
22
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
23
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
24
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1) Categoria de
pacient din registrul de tuberculoza N = caz nou; R = recidivid; E =
retratament dupa esec; A = retratament dupa abandon; C = cronic
2) Categoria de
evaluare acazului de MDR TB: T = tratament complet; E = esec; A = abandon; D
=deces; M = mutat; P = pierdut
Tipărit cu suportul financiar al Organizatei
Mondiale a Sanatatii - Biroul pentru Controlul Tuberculozei in Balcani
FIŞA DE MONITORIZARE A EVOLUŢIEI SUB TRATAMENT A
PACIENTULUI CU TUBERCULOZĂ MULTIDROG REZISTENTĂ (MDR TB)
|
Nume, prenume............................................................................................
Adresa.........................................................................................................
Sex..............................M / F.....................................Vârsta........................
Diagnostic....................................................................................................
...................................................................................................................
|
|
Nr registru MDR
.....................................
Dispensar TB
.....................................
Judeţ.............................
|
|
Tipul de pacient MDR
|__| caz nou
MDR, netratat anterior pentru tuberculoză
|__| caz de MDR TB, tratat anterior cu
medicamente de linia I (>1 lună)
|__| caz: de MDR TB, tratat anterior
cu medicamente de linia a II-a (>1 luna)
|
|
Luna de
tratament
|
Rezultatele
examenului bacteriologic
|
Rezultatele
antibiogramei (ABG)
|
G kg
|
RX
(trimestrial)
|
|
Data
|
Nr. lab.
|
Rezult.
ex. direct
|
Data
obţinerii culturii
|
Rezultat
cultura
|
Data
obţinerii ABG
|
H
|
R
|
Z
|
E
|
S
|
Km Ak
|
Cpm
|
QCpx Ofx
|
Etm
Ptm
|
Ce
|
Pas
|
|
|
TO
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T1
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T2
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T3
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T4
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T5
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T6
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T7
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T8
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T9
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T10
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T11
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T12
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T13
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T14
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T15
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T16
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T17
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T18
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T19
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T20
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T21
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T22
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T23
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T24
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tipărit cu suportul financiara Organizaţiei Mondiale
a Sănatătii Biroul pentru Controlul Tuberculozei in Balcani
*) Anexa nr. 12 este reprodusă în facsimil.
ANEXA Nr. 13*) la normele metodologice
Judetul
:.....................................................................
Disp.
Pneumoftiziologice............................................
Fisa de evauare a tratamentului antituberculos
Cod pacient
:.......................................................
Nume.
prenume.............................................................................................................
CNP:.......................................
Sex:............................. Data nasterii.............................
Judet nastere........................................Loc
nastere........................................................
Cetatenie: .............................................................
Varsta..............................................
Dta
declarare......................................................Nr. registru
dispensar...........................
Categorie caz .......................................................Localizare.........................................
Diagnostic principal:
.......................................................................................................
Diafnostic secundar:........................................................................................................
Exanene bacteorologice
Antibiograma

Spitalizari:
|
Spital/Sanatoriu
|
Data internarii
|
Data externarii
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tratament
|
Tip regim
|
Data incepere
|
Asocierea
|
Ritm
|
Data incheiere
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Evaluare:........................................................
Data evaluarii:..............................
Data
completarii.............................................. Madic:........................................
ANEXA Nr. 14 la normele metodologice
TEHNICA VACCINĂRII BCG
In România, vaccinarea BCG se
va efectua cu o tulpină evaluată periodic pentru calitatea produsului.
Vaccinul liofilizat se prezintă ca o suspensie de 1
mg/ml CG pe mediu Sauton, în soluţie protectoare de glutamat de sodiu 1,5%.
Produsul conţine aproximativ 4-5 milioane de germeni/1g de vaccin. Vaccinarea
se efectuează numai de către personal mediu special instruit, sub responsabilitatea
medicală şi legală a medicului. Fiola vidată în care se găseşte pulberea
vaccinală se deschide sub protecţia foliei existente în ambalaj pentru a
preveni răspândirea conţinutului la pătrunderea aerului, după care se suspendă
în 2 ml mediu Sauton anexat. Suspensia obţinută, claropalescentă, se barbotează
până la omogenizare şi se utilizează în maximum 30 de minute. Fiola conţine
aproximativ 20 de doze vaccinale, dar pierderile pe ac împiedică un număr
echivalent de vaccinări. Produsul neutilizat se inactivează şi se aruncă.
Păstrarea vaccinului este obligatorie la întuneric şi la 4°C, în caz contrar degradându-se şi putând conduce
la eşecuri vaccinale.
Vaccinarea constă în injectarea strict intradermic a
0,1 ml (0,1 mg BCG) suspensie vaccinală, în treimea superioară a braţului
stâng, pe faţa postero-externă, după dezinfecţia tegumentelor. Dacă tehnica a
fost corectă, se obţine o papulă cu diametrul de 5-6 mm cu aspect de „coajă de
portocală", care nu se tamponează.
Contraindicaţiile vaccinării BCG a nou-născutului:
- temporare: starea febrilă, leziunile tegumentare
eruptive, greutate sub 2.500 g;
- absolute: infecţia HIV simptomatică, imunodeficienţe
(congenitale, leucemii, limfoame, neoplazii generalizate), tratamente
imunosupresoare cu corticosteroizi, agenţi alkilanţi, antimetaboliti etc.
ANEXA Nr. 15*) la normele metodologice
FIŞA PENTRU CHIMIOPROFILAX1E
Dispensarul de pneumoftiziologie
..................................................................
Judetul..........................................................................................................
Caz sursa:
Nume....................................Prenume........................
Cod pacient...........................Nr.
registru..............Data declararii
FIŞA DE CHIMIOPROFILARE
Nume ........................................ Prenume
.........................................................
CNP.........................................
Sex..............Data nasterii................................
Adresa...............................................................................................................
|
Data
|
Examene,rezultate, tratamente,
|
|
|
|
|
Data
|
Examene, rezultate, tratament
|
|
|
|
Tipărit cu suportul financiara Organizaţiei Mondiale
a Sănatătii Biroul pentru Controlul Tuberculozei in Balcani
ANEXA Nr. 16 la normele metodologice
IDEILE PRINCIPALE
pentru discuţia cu pacienţii la diferite momente ale
tratamentului si în situaţii particulare
Teme de bază de discutat la prima întâlnire cu pacientul
după stabilirea diagnosticul de TB
Prima întâlnire cu pacientul
oferă ocazia de a comunica informaţii importante despre TB si tratamentul său.
La prima întâlnire cu un
pacient cu TB trebuie discutate următoarele teme importante:
- ce este TB;
- TB este curabilă:
- tratamentul TB;
- necesitatea urmăririi directe
a tratamentului;
- modul de răspândire a TB;
- simptome;
- modalităţi de prevenire a transmiterii;
- importanţa tratamentului complet;
- la ce să se aştepte, ce este de făcut în continuare;
- importanţa colaborării la controlul contacţilor
(familiali, de colectivitate, de anturaj).
*) Anexele nr. 13 şi 15 sunt reproduse în facsimil
Teme de bază care trebuie subliniate pe parcursul
tratamentului
Educarea pacientului este un proces continuu de-a
lungul terapiei. După întâlnirea iniţială cu acesta, mesajele educaţionale
trebuie transmise continuu şi întărite. Următoarele teme sunt considerate ca
fiind relevante:
- tipul şi culoarea medicamentelor/soluţiilor
injectabile;
- cantitatea şi frecvenţa administrării;
- efectele secundare;
- tratamentul de continuare;
- frecvenţa şi importanţa examenelor de spută şi
semnificaţia rezultatelor acestora;
- consecinţele luării numai unuia dintre medicamente
sau ale opririi tratamentului;
- ce se întâmplă dacă pacientul vrea să se mute în
timpul tratamentului.
Ce este de spus sau
de făcut atunci când:
Pacientul se simte mai bine şi vrea să întrerupă
tratamentul.
Trebuie explicat că simptomele se pot ameliora sensibil
în faza iniţială a tratamentului (primele 8 săptămâni).
Totuşi, dacă pacientul nu continuă tratamentul în
următoarele 6 luni, unii bacili tuberculoşi pot supravieţui, inducând recăderea
şi dezvoltarea de microorganisme rezistente la medicatie. Chiar dacă pacientul
se simte mai bine, este important să îşi continue tratamentul.
Un pacient nou vrea să îşi ia medicaţia acasă (fără
supraveghere).
Puneţi întrebări pentru a determina cauzele acestei
decizii. Explicaţi că majoritatea pacienţilor nou-diagnosticaţi sunt
spitalizaţi în timpul fazei intensive a tratamentului, pentru a putea fi monitorizaţi cu atenţie. In timpul
fazei de continuare, dacă este dificilă venirea la dispensar, întrebaţi dacă
există sprijin din partea familiei faţă de tratament. Explicaţi că există o
politică fermă în a insista ca tratamentul să fie monitorizat direct.
Pacientul a lipsit de la tratament două zile în timpul fazei de continuare (a omis două prize
din tratament).
Aflaţi motivele. Incercaţi să rezolvaţi problemele.
Amintiţi-le atât pacientului, cât şi aparţinătorilor/părinţilor despre
necesitatea de a lua toate dozele pe durata tratamentului. Recuperaţi priza
pierdută.
Pacientul nu vrea să facă examenul de spută după 5
luni de tratament.
Explicaţi necesitatea examenului. Spuneţi atât
pacientului, cât şi aparţinătorilor/părinţilor că este important să fim siguri
că tratamentul progresează favorabil.
Mama copilului spune că soţul ei, care tuşeşte, nu
are timp pentru investigarea TB.
Aflaţi dacă mama a comunicat soţului că copilul are TB.
Explicaţi că este important pentru el să fie testat, deoarece i-ar putea
infecta şi pe alţii sau ar putea-o reinfecta pe mamă ori pe copil. Oferiţi-vă
să îl vizitaţi pe soţ sau aranjaţi cu un coleg să îl viziteze şi să îi explice
necesitatea controlării.
Mama se teme să spună familiei că copilul are TB.
Oferiţi-vă să vorbiţi cu familia despre TB. Liniştiţi
familia: copilul nu este contagios, el fiind în tratament. Explicaţi modul de
transmitere şi modalităţile de prevenire a TB.
Pacientul se simte rău din cauza tratamentului şi
vrea să îl oprească.
Stabiliţi dacă simptomele pacientului sunt cauzate de
medicaţia anti TB şi dacă reprezintă efecte adverse minore sau majore ale
acesteia. Dacă sunt efecte majore, opriţi tratamentul şi trimiteţi pacientul la
DPR Dacă sunt efecte minore, ajutaţi-l să le facă faţă, astfel încât să îşi
continue tratamentul. Explicaţi părinţilor importanţa tratamentului corect.
Pacientul nu are mijloace de transport pentru a veni
la dispensar.
Aflaţi motivele. Incercaţi să conlucraţi cu pacientul/părinţii
în găsirea unor soluţii. Cereţi sprijinul autorităţilor locale pentru a rezolva
problema.
ANEXA Nr. 17*) la normele metodologice
REGISTRUL DE LABORATOR

*) Anexa nr. 17 este reprodusă în facsimil.
ANEXA Nr. 78 la normele metodologice
INDICATORII UTILIZAŢI
la monitorizarea şi evaluarea PNCT
I. Indicatori-cadru de evaluare ai PNCT
Raportare la ANP (subprogramul 2.3); vezi cap.
„Raportări statistice".
Indicatori fizici -
trimestrial/anual:
• numărul contactilor examinaţi (valoare optimă: 4
contacţi/1 caz de TB înregistrat);
• numărul de suspecţi (simptomatici) examinaţi (valoare
optimă: 10 suspecţi/1 caz de TB înregistrat);
• numărul cazurilor care beneficiază de
chimioprofilaxie (minimum 1/1 caz de TB înregistrat);
• numărul de intradermoreactii la PPD efectuate: (3/1
caz TB de înregistrat, în funcţie de vârsta contactilor);
• numărul de vizite de supervizare în teritoriu
efectuate de către medicii specialişti;
• numărul de vizite de supervizare în cadrul judeţelor;
• numărul de activităţi de IEC.
Indicatori de eficienţă
- trimestrial/anual:
• cost mediu cu depistarea activă
a bolnavului cu TB prin controlul contactilor şi al altor grupe de risc;
• cost mediu al bolnavului cu TB prin controlul
simptomaticilor;
• cost mediu/tratament chimioprofilactic;
• cost mediu al intradermoreacţiei la PPD;
• cost mediu pe vizită de supervizare
în teritoriu;
• cost mediu/campanie IEC.
Indicatori de rezultat -
anual:
• procentul contactilor examinaţi din totalul
contactilor înregistraţi > 80%;
• procentul bolnavilor depistaţi din numărul
suspecţilor examinaţi > 10%;
• procentul persoanelor chimioprofilactizate din cele
indicate pentru chimioprofilaxie > 90%;
• procentul de vizite efectuate din numărul de vizite
programate > 80%;
• procentul de campanii de IEC efectuate din numărul de
campanii programate > 80%.
II. Indicatori specifici de monitorizare
Raportare la CASJ
Indicatori fizici -
lunar/trimestrial/anual:
• numărul de bolnavi cu TB trataţi: cazuri noi,
recidive, tratamente individualizate;
• numărul cazurilor cu chimioterapie preventivă (TB
latentă);
• numărul de investigaţii radiologice
efectuate;
• numărul de investigaţii bacteriologice efectuate.
Indicatori de eficienţă
- anual:
• cost mediu/bolnav de TB tratat/an;
• cost mediu/pacient cu chimioterapie preventivă (TB
latentă)/an;
• cost mediu pentru cazuri noi, recidive, tratament
individualizat/an;
• cost mediu al investigaţiei radiologice;
• cost mediu al unei investigaţii bacteriologice.
Indicatori de rezultat -
activitate profilactică şi curativă:
• rata de notificare a cazurilor noi şi a recidivelor
să nu depăşească 130 %ooo;
• rata de conversie a sputei la două luni a cazurilor
noi pulmonare > 75%;
• rata de succes terapeutic a cazurilor noi confirmate
bacteriologic > 80%;
• corecta încadrare a bolnavilor (%);
• cazurile de TB pulmonară cavitară neconfirmate
bacteriologic din total cazuri de TB pulmonară;
• cazurile de TB grave la copii: meningite, miliare din
total cazuri de TB la copii;
• numărul de beneficiari ai PNCT: bolnavi +
simptomatici/suspecţi/contacţi investigaţi;
• numărul de cazuri de TB identificate din contacţii
examinaţi în urma AE;
• bugetul pe surse de finanţare.
Indicatori ai procesului de formare:
• numărul de sesiuni de curs pentru medici
pneumologi/an;
• numărul de sesiuni de curs pentru personal de
laborator/an;
• numărul de sesiuni de curs pentru specialişti
epidemiologi/an;
• numărul de sesiuni de curs pentru asistenţii medicali
din reţeaua de pneumologie/an;
• numărul de sesiuni de curs pentru MF/an;
• numărul de sesiuni de curs pentru asistenţii medicali
din afara reţelei/an;
• numărul de medici pneumologi care au urmat cursuri de
învăţământ la distanţă/an;
• numărul de asistenţi medicali din cadrul reţelei de
pneumologie care au urmat cursuri de învăţământ la distanţă/an;
• numărul de persoane-cheie implicate în PNCT care au
participat la cursuri internaţionale/an.
Indicatori de monitorizare a intervenţiilor pentru
schimbarea comportamentelor:
• numărul de broşuri „Ghidul pacientului TB
(adulţi)" publicate/an;
• numărul de broşuri „Ghidul pacientului TB
(copii)" publicate/an;
• numărul de persoane care accesează site-ul
www.tuberculoza.ro/lună;
• numărul de conferinţe organizate cu ocazia Zilei mondiale
de luptă împotriva TB;
• numărul de abandonuri înregistrate/an;
• numărul de pacienţi care au primit bonuri valorice
pentru alimente şi au terminat cu succes tratamentul/an.
Indicatori de monitorizare a supervizării:
• numărul de DPF vizitate de două ori/an din totalul
dispensarelor (%);
• numărul de cabinete MF vizitate anual.
III. Indicatori epidemiometrici
Evaluarea endemiei de TB şi a impactului aplicării PNCT
la toate nivelurile (DPF, judeţean, sau la nivel naţional) se face prin
prelucrarea datelor (total cazuri noi/recidive) pe cohorte*) de bolnavi, cu
ajutorul următorilor indicatori:
|
Incidenţa cazurilor noi
pulmonare pozitive la microscopie
|
=
|
____nr. cazuri noi cu TB pulmonară, pozitivă la
microscopie ______
nr. locuitori din teritoriul respectiv la data de 1
iulie a anului respectiv
|
x 100.000
|
Această incidenţă se poate calcula şi specific, pe sexe
şi grupe de vârste.
|
Incidenţa TB la copii
|
=
|
______________nr. cazuri TB la copii ( 0 -15 ani)
_______________
nr. copii (0-15 ani) din teritoriul respectiv la data de 1 iulie a
anului respectiv
|
x 100.000
|
Incidenţa se poate recalcula la sfârşitul anului
următor, excluzând din numărul de cazuri numărul de infirmaţi din categoria
respectivă de bolnavi.
|
Indice meningitic la copii
|
=
|
_nr. cazuri meningită TB
nr. cazuri TB la copii
|
x 100
|
|
Mortalitatea
|
=
|
________________nr. decese prin TB______________________
nr. locuitori din teritoriul respectiv la data de 1 iulie a anului
respectiv
|
x 100.000
|
|
Prevalenta periodică
|
=
|
________nr. bolnavi TB înregistraţi în perioada analizată
________
nr. locuitori din teritoriul respectiv la data de 1 iulie a anului
respectiv
|
x 100.000
|
|
Prevalenta instantanee
|
=
|
______nr. bolnavi aflaţi în tratament la un moment dat __________
nr. locuitori din teritoriul respectiv la data de 1 iulie a anului
respectiv
|
x 100.000
|
* Cohortă - un grup de pacienţi înregistraţi şi declaraţi într-o perioadă de
timp dată (trimestru, an), care urmează a fi evaluaţi pe baza unor criterii
prestabilite.
IV. Indicatori de monitorizare ai PNCT privind
diagnosticul
|
Rata de depistare a cazurilor noi pulmonare
microscopic pozitive din cazurile suspecte examinate - indicator calculat de
OMS, disponibil în Raportul anual global de control al tuberculozei
|
=
|
nr. cazuri noi pulmonare pozitive la microscopie
depistate
nr. cazuri noi pulmonare pozitive la microscopie
estimate anual
|
x 100
|
Rata de confirmare bacteriologică a cazurilor
pulmonare:
|
prin microscopie
|
=
|
___nr. cazuri cu TB pulmonară M+ __
nr. cazuri înregistrate cu TB
pulmonară
|
x 100
|
|
prin cultură
|
=
|
___nr. cazuri cu TB pulmonară C+ __
nr. cazuri înregistrate cu TB pulmonară
|
x 100
|
Indicatorul se poate calcula global, pentru toate
cazurile cu TB pulmonară înregistrate, sau separat pentru cazuri noi şi
recidive pulmonare (rata de confirmare a cazurilor pulmonare, a celor noi,
respectiv a recidivelor pulmonare, prin microscopie sau prin cultură).
In centrele în care diagnosticul bacteriologic este
corespunzător, proporţia cazurilor pozitive în microscopie raportată la toate cazurile pulmonare este de peste 60%.
|
Proporţia cazurilor cu TB pulmonară negative în
microscopie şi pozitive în cultură
|
=
|
nr. cazuri pulmonare negative la microscopie şi
pozitive la cultură
nr. cazuri înregistrate cu TB pulmonară pozitive la
cultură
|
x 100
|
Indicatorul arată aportul examenului prin cultură la
confirmarea bacteriologică a cazurilor pulmonare. Valoarea lui trebuie să fie
sub 25%.
|
Procentul cazurilor cu TB extrapulmonară
|
=
|
_nr. cazuri cu TB extrapulmonară__
nr. total de cazuri cu TB înregistrate
|
x 100
|
TB extrapulmonară trebuie să reprezinte un procent mic
(în jur de 10%) din totalul cazurilor cu TB. Procente mai mari sau mai mici pot
sugera deficienţe în stabilirea diagnosticului de TB extrapulmonară sau în
detecţia şi supravegherea cazurilor cu TB pulmonară.
|
Procentul cazurilor infirmate
|
=
|
nr. cazuri înregistrate cu TB pulmonară, ulterior
infirmate
nr. total de cazuri de TB înregistrate
|
x 100
|
|
Seroprevalenţa infecţiei HIV în rândul cazurilor noi
cu TB pulmonară microscopic
pozitive
|
=
|
nr. cazuri noi cu TB pulmonară pozitive în
microscopie, care sunt HIV pozitive
nr. total cazuri noi pulmonare microscopic
pozitive, testate HIV
|
x 100
|
Indicatorul este util pentru a corobora datele de
supraveghere privind incidenţa TB cu cele privind prevalenta infecţiei HIV în
rândul populaţiei.
V Indicatori de monitorizare ai PNCT privind
rezultatele tratamentului
|
Procentul cazurilor noi de TB
|
=
|
__nr.cazuri noi de TB înregistrate __
nr. total de cazuri cu TB înregistrate
|
x 100
|
Indicatorul evidenţiază indirect calitatea
tratamentelor antituberculoase administrate, având în vedere că o bună calitate
a acestora determină creşterea proporţiei de cazuri noi faţă de retratamente.
Indicatorul aduce, de asemenea, informatii despre
extinderea transmisiei recente a TB in randul populatiei
|
Procentul cazurilor cu MDR-TB
|
=
|
_________nr. cazuri de MDR-TB înregistrate
__________
nr. total de cazuri cu TB
pulmonară cu antibiogramă efectuată
|
x 100
|
Indicatorul reprezintă procentul de cazuri cu TB
pulmonară care sunt rezistente cel puţin la Izoniazidă şi Rifampicină şi
evidenţiază indirect eficacitatea aplicării PNCT, având în vedere că o bună
funcţionare a PNCT determină un număr limitat al acestor cazuri.
|
Rata de conversie a sputei la sfârşitul a două luni
de tratament pentru cazurile noi pulmonare pozitive în microscopie
|
=
|
nr. cazuri noi de TB pulmonară microscopic pozitive,
care s-au negativat la microscopie la sfârşitul a două luni de tratament
___________________________________________________________________
nr. total cazuri noi
pulmonare microscopic pozitive
|
x 100
|
După două luni de tratament, peste 85% din cazurile
iniţial pozitive la microscopie ar trebui să fie negativate.
|
Rata de bactericidie în spută
|
=
|
nr. cazuri noi de TB pulmonară pozitive la cultură,
care au cultură negativă la sfârşitul a două luni de tratament
__________________________________________________________________________________
nr. total cazuri noi pulmonare pozitive la cultură
|
x 100
|
Cei 2 indicatori (rata de conversie a sputei şi rata de
bactericidie în spută) măsoară procentul de cazuri noi pulmonare pozitive în
microscopie, respectiv cultură, care au o mare probabilitate de vindecare la
încheierea tratamentului.
Majoritatea cazurilor noi de TB
pulmonară pozitive în microscopie/cultură trebuie să se negativeze în
microscopie/cultură la sfârşitul a două luni de tratament. O rată scăzută de
conversie/bactericidie la două luni de tratament poate avea ca semnificaţie o
rată înaltă de chimiorezistenţă primară şi/sau o incidenţă mare a formelor
severe de boală.
|
Procentul de cazuri noi pulmonare microscopic pozitive
care sunt vindecate (rata de vindecare)
|
=
|
nr. cazuri noi cu TB pulmonară microscopic pozitive
care au fost vindecate
________________________________________________________
nr. total cazuri noi pulmonare
microscopic pozitive evaluabile
|
x 100
|
Indicatorul măsoară direct succesul PNCT în vindecarea
cazurilor cu TB pulmonară confirmată microscopic.
|
Procentul de cazuri noi pulmonare pozitive în
microscopie, cu tratament încheiat (rata de tratamente încheiate)
|
=
|
nr. cazuri noi cu TB pulmonară microscopic pozitive,
cu tratament încheiat
________________________________________________________
nr. total cazuri noi pulmonare microscopic
pozitive evaluabile
|
x 100
|
Indicatorul măsoară capacitatea PNCT în privinţa
obţinerii tratamentului încheiat la pacienţii care nu pot fi evaluaţi ca
vindecaţi.
Când vindecarea nu poate fi stabilită, tratamentul încheiat
este cel mai bun mod prin care putem fi siguri că pacienţii au fost trataţi
adecvat.
|
Procentul de cazuri noi pulmonare pozitive în
microscopie care au fost tratate cu succes (rata de succes terapeutic)
|
=
|
nr. cazuri noi de TB pulmonară microscopic pozitive care au fost
vindecate sau au tratament încheiat
nr. total cazuri noi pulmonare microscopic
pozitive evaluabile
|
x 100
|
Prin combinarea celor două tipuri de evaluare a
rezultatelor tratamentelor se poate determina rata de succes terapeutic.
Indicatorul măsoară eficacitatea PNCT în ceea ce priveşte rezultatele
tratamentelor antituberculoase.
PNCT, care va atinge o rată de succes la cazurile noi
pulmonare pozitive la microscopie de cel puţin 85% şi o rată de detecţie a
aceluiaşi tip de cazuri de 70%, va obţine scăderea rapidă a mortalităţii prin
TB, a prevalentei şi a transmisiei bolii, a numărului de cazuri cu
chimiorezistenţă.
|
Procentul de cazuri noi pulmonare pozitive în
microscopie care au decedat (rata de deces sau fatalitatea)
|
=
|
nr. cazuri noi cu TB pulmonară microscopic
pozitive care au decedat în timpul tratamentului
_________________________________________
nr. total cazuri noi pulmonare microscopic pozitive
evaluabile
|
x 100
|
Este unul dintre indicatorii posibili de evaluare a
rezultatelor tratamentelor pacienţilor cu TB.
Pacienţii care decedează din orice motiv în timpul tratamentului, precum şi cei
care sunt înregistraţi post-mortem sunt evaluaţi ca decedaţi. Indicatorul
include toate cauzele de deces şi de aceea, dacă fatalitatea este mare (peste
5%), pentru acurateţea interpretării, este util să se facă separarea deceselor
prin TB de cele prin alte cauze.
Dacă fatalitatea prin TB creşte, este necesar să fie
analizate cauzele deceselor pentru a se determina dacă acestea pot fi
prevenite.
|
Procentul de cazuri noi
pulmonare pozitive în microscopie care au fost eşecuri ale tratamentului
(rata de eşec)
|
=
|
nr. cazuri noi de TB pulmonară microscopic pozitive
care au fost eşecuri ale tratamentului
___________________________________________________________________
nr. total cazuri noi pulmonare
microscopic pozitive evaluabile
|
x 100
|
Când rata de eşec al tratamentului depăşeşte un anumit
procent (faţă de un procent acceptabil), algoritmul de diagnostic bacteriologic
şi cel de tratament trebuie revăzute, pentru a se stabili cauza eşecurilor şi
dacă acestea pot fi prevenite.
|
Procentul de cazuri noi pulmonare pozitive în
microscopie care au abandonat tratamentul (rata de abandon)
|
=
|
nr. cazuri noi de TB pulmonară microscopic pozitive
care au abandonat tratamentul
_______________________________________________________________
nr. total cazuri noi pulmonare
microscopic pozitive evaluabile
|
x 100
|
In situaţia în care rata abandonurilor este mare (faţă
de un procent acceptabil), se vor face investigaţii suplimentare pentru a se
determina dacă aceste abandonuri pot fi prevenite.
|
Procentul de cazuri noi
pulmonare pozitive în microscopie care au fost pierdute din observaţie (rata
pierduţilor)
|
=
|
nr. cazuri noi de TB pulmonară microscopic
pozitive
care au abandonat tratamentul şi sunt pierdute din
observaţie
______________________________________________
nr. total cazuri noi pulmonare microscopic pozitive
evaluabile
|
x 100
|
In situaţia în care rata pierduţilor este mare (faţă de
un procent acceptabil), se vor face investigaţii pentru a se determina cauza şi
se vor lua măsuri pentru ca aceste pierderi să fie prevenite.
|
Procentul de cazuri noi pulmonare pozitive în
microscopie care s-au mutat într-un alt dispensar (rata de
„transfer-aut")
|
=
|
nr. cazuri noi de TB pulmonară microscopic pozitive
care s-au mutat într-un alt dispensar
______________________________________________
nr. total cazuri noi pulmonare microscopic pozitive
evaluabile
|
x 100
|
|
Procentul de cazuri noi pulmonare pozitive în
microscopie care continuă tratamentul la 12 luni (rata celor care continuă
tratamentul)
|
=
|
nr. cazuri noi de TB pulmonară microscopic pozitive
care continuă tratamentul la 12 luni
__________________________________________________________________
nr. total cazuri noi pulmonare
microscopic pozitive evaluabile
|
x 100
|
Acest procent trebuie să fie practic egal cu cel al
cazurilor cu MDR-TB, la care tratamentul antituberculos indicat este de cel
puţin 24 de luni. Dacă procentul este mai mare, se vor analiza motivele
continuării unui număr mare de tratamente peste 12 luni.
Pentru cuprinderea tuturor cazurilor unei cohorte,
analiza rezultatelor tratamentelor se face la 12 luni de la înregistrarea şi declararea ultimului caz din cohorta
respectivă.
Numărul cazurilor evaluate trebuie să fie egal cu
numărul cazurilor evaluabile, astfel încât suma procentelor calculate pentru
fiecare categorie de evaluare să fie egală cu 100.
Analiza se face în acelaşi fel
şi pentru alte categorii de cazuri:
• cazuri noi pulmonare pozitive în cultură;
• recidive pulmonare pozitive la microscopie sau în
cultură;
• total retratamente;
• cazuri noi pulmonare neconfirmate bacteriologic;
• cazuri extrapulmonare etc.
Rezultatele pot fi redate atât tabelar, cât şi grafic,
pentru un moment dat sau în dinamică.
Indicatorii de evaluare ai PNCT se raportează anual.
Indicatorii raportaţi trimestrial către ANP vor fi
trimişi obligatoriu şi la UCM.