LEGE Nr. 178
din 18 octombrie 2000
privind produsele cosmetice
ACT EMIS DE:
PARLAMENTUL ROMANIEI
ACT PUBLICAT IN:
MONITORUL OFICIAL NR. 120 din 16 februarie 2011
CAPITOLUL I
Dispoziţii generale
Art. 1. - Prezenta lege reglementează condiţiile care
trebuie să fie respectate la fabricarea şi punerea pe piaţă a produselor
cosmetice de uz uman.
Art. 2. - (1) Pentru aplicarea
prezentei legi termenii şi sintagmele de mai jos semnifică după cum urmează:
a) produs cosmetic -
orice substanţă sau amestec care urmează să fie pus în contact cu diverse părţi
externe ale corpului uman, precum piele, păr, unghii, buze, organe genitale
externe sau cu dinţii şi mucoasa bucală, cu scopul exclusiv sau principal de a
le curăţa, a le parfuma, a le modifica aspectul şi/sau a le corecta mirosurile
corporale şi/sau a le proteja ori a le menţine în bună stare;
b) coloranţi cosmetici - substanţe care se adaugă în
produse cosmetice în scopul colorării produsului şi/sau a unor părţi ale
corpului uman;
c) conservanţi - substanţe care se adaugă în produsele cosmetice, în scopul
principal de a inhiba dezvoltarea microorganismelor în aceste
produse;
d) filtre ultraviolete -
substanţe care se adaugă în produsele cosmetice pentru a filtra anumite
radiaţii ultraviolete, în scopul protejării pielii de efectele nedorite ale
acestor radiaţii;
e) lot de fabricaţie - o cantitate definită în materie primă, material de ambalare sau
produs finit, fabricată în condiţii identice printr-un proces sau o serie de
procese, astfel încât să poată fi considerată omogenă;
f) număr de lot de
fabricaţie - o combinaţie distinctivă de numere
şi/sau de litere, care în mod specific identifică un lot;
g) dată de minimă
durabilitate - data până la care un produs,
depozitat în condiţii corespunzătoare, continuă să îşi îndeplinească
funcţiunile iniţiale şi respectă prevederile art. 5;
h) notificare - demersul administrativ care constă în transmiterea în formă scrisă către Ministerul
Sănătăţii a intenţiei de punere pe piaţă a unui produs cosmetic;
i) principii de bună
practică de fabricaţie a produselor cosmetice -
ansamblul de reguli care grupează principii generale, proceduri, acţiuni şi
verificări ce se exercită asupra procesului de fabricaţie a produselor cosmetice;
j) etichetă - orice material scris care conţine elemente de identificare a
produsului şi, după caz, instrucţiuni de utilizare pentru consumator;
k) ambalaj primar-
material care vine în contact direct cu produsul cosmetic, folosit la
menţinerea caracteristicilor prescrise ale produsului pe toată perioada de
valabilitate;
l) ambalaj secundar - material folosit la
protejarea ambalajului primar;
m) perioada după
deschidere - perioada de timp în care un produs
cosmetic finit poate fi folosit în siguranţă, calculată din momentul primei
deschideri a ambalajului primar şi începerii utilizării produsului.
(2) Pentru aplicarea prevederilor art. 8 şi ale art.
19, următorii termeni şi expresii se definesc după cum urmează:
a) produs cosmetic finit - produsul cosmetic în formula sa finală, aşa cum este pus pe piaţă
şi oferit consumatorului final, sau prototipul acestuia;
b) prototip - primul model sau proiect al unui produs cosmetic care nu a fost fabricat în loturi şi de la care
produsul cosmetic finit este copiat sau dezvoltat.
(3) Pentru aplicarea prevederilor art. 7, următoarea
expresie se defineşte astfel:
- ingredient cosmetic -
orice substanţă chimică sau amestec de origine sintetică ori naturală folosit
în compoziţia unui produs cosmetic, cu excepţia compoziţiilor de parfumare şi
aromatizare.
Art. 3. - Lista cuprinzând categoriile de produse
cosmetice, aşa cum sunt definite în cuprinsul art. 2 alin. (1) lit. a), este
prevăzută în anexa nr. 1.
Art. 4. - Ministerul Sănătăţii reprezintă autoritatea
naţională competentă pentru reglementarea comercializării produselor cosmetice,
notificarea acestora în întocmirea şi administrarea bazei de date, inspecţia şi
controlul pe piaţă, informarea populaţiei, înregistrarea cazurilor semnalate
privind efectele adverse asupra populaţiei, cauzate de produsele cosmetice,
raportarea către Comisia Europeană.
CAPITOLUL II
Condiţii impuse produselor cosmetice pentru
securitatea consumatorilor
Art. 5. - Produsele cosmetice puse pe piaţă nu trebuie
să pericliteze sănătatea umană atunci când sunt folosite în condiţii normale
sau previzibile în mod rezonabil de folosire, ţinându-se seama, în special, de
prezentarea produsului, etichetarea, instrucţiunile privind păstrarea şi
utilizarea acestuia, precum şi de orice altă indicaţie sau informaţie prevăzută
de producător, de reprezentantul său autorizat sau de orice altă persoană
responsabilă pentru punerea pe piaţă a produsului. Aceste indicaţii sau
informaţii nu vor scuti nicio persoană, în nicio circumstanţă, să se conformeze
altor dispoziţii ale prezentei legi.
Art. 6. - Ministerul Sănătăţii ia toate măsurile
necesare pentru a fi puse pe piaţă numai acele produse care se conformează
prevederilor prezentei legi şi ale Ordinului ministrului sănătăţii nr.
1.448/2005 privind categoriile de produse cosmetice şi listele cuprinzând
substanţele ce pot fi utilizate în compoziţia produselor cosmetice, cu
modificările şi completările ulterioare.
Art. 7. - (1) Fără a afecta
aducerea la îndeplinire a obligaţiilor prevăzute la art. 5, se interzice
punerea pe piaţă a produselor cosmetice în a căror compoziţie se găsesc:
a) substanţe prevăzute în anexa nr. II la Ordinul ministrului sănătăţii nr.
1.448/2005, cu modificările şi completările ulterioare;
*) Republicată în temeiul art. III din Legea nr.
260/2010 pentru abrogarea art. 8 din Legea nr. 178/2000 privind produsele
cosmetice, publicată în Monitorul Oficial al României, Partea I, nr. 848 din 17 decembrie 2010, dându-se
textelor o nouă numerotare.
Legea nr. 178/2000 privind produsele cosmetice a mai
fost republicată în Monitorul Oficial al României, Partea I, nr. 91 din 27 ianuarie 2005, iar
ulterior a mai fost modificată şi completată prin:
- Legea nr. 469/2006 pentru
modificarea şi completarea Legii nr. 178/2000 privind produsele cosmetice,
publicată în Monitorul Oficial al României, Partea I,
nr. 1.029 din 27 decembrie 2006;
- Ordonanţa Guvernului nr. 2/2010 pentru modificarea
Legii nr. 178/2000 privind produsele cosmetice, publicată în Monitorul Oficial
al României, Partea I, nr. 59
din 26 ianuarie 2010, aprobată prin Legea nr. 159/2010, publicată în Monitorul
Oficial al României, Partea I, nr. 496 din 19 iulie
2010.
b) substanţe în afara limitelor de admisibilitate şi a
condiţiilor prevăzute în anexa nr. III, Partea 1, la Ordinul ministrului
sănătăţii nr. 1.448/2005, cu modificările şi completările ulterioare;
c) agenţi de colorare, alţii decât cei prevăzuţi în
anexa nr. IV, Partea 1, la Ordinul ministrului sănătăţii nr. 1.448/2005, cu modificările şi completările
ulterioare, cu excepţia produselor cosmetice destinate a fi folosite numai la
colorarea părului;
d) agenţi de colorare prevăzuţi în anexa nr. IV, Partea 1, la Ordinul ministrului
sănătăţii nr. 1.448/2005, cu modificările şi completările ulterioare, în alte
condiţii decât cele specificate, cu excepţia produselor cosmetice destinate a
fi folosite numai la colorarea părului;
e) conservanţi, alţii decât cei stabiliţi în anexa nr. VI, Partea 1, la Ordinul ministrului
sănătăţii nr. 1.448/2005, cu modificările şi completările ulterioare;
f) conservanţi, în afara
limitelor de admisibilitate şi a condiţiilor impuse de anexa nr. VI, Partea 1, la Ordinul ministrului
sănătăţii nr. 1.448/2005, cu modificările şi completările ulterioare, cu
excepţia cazului în care sunt folosite alte concentraţii, pentru scopuri
specifice, care rezultă din prezentarea produsului;
g) filtre UV, altele decât cele stabilite în anexa nr.
VII, Partea 1, la Ordinul ministrului sănătăţii nr. 1.448/2005, cu modificările
şi completările ulterioare;
h) filtre UV, folosite în afara limitelor de
admisibilitate şi a condiţiilor impuse în anexa nr. VII, Partea 1, la Ordinul
ministrului sănătăţii nr. 1.448/2005, cu modificările şi completările ulterioare.
(2) Prezenţa urmelor unor substanţe dintre cele prevăzute
la alin. (1) lit. a) este permisă numai dacă, din punct de vedere tehnic, nu
poate fi evitată în condiţiile unei bune practici de fabricaţie şi se respectă
prevederile art. 5.
(3) Prevederile Ordinului
ministrului industriei şi resurselor şi al ministrului sănătăţii şi familiei
nr. 309/729/2001 privind inventarul pentru ingredientele folosite în produsele
cosmetice au valoare indicativă, fără să constituie o listă a substanţelor
autorizate pentru a fi folosite în produsele cosmetice.
Art. 8. - (1) Fără a se afecta aducerea la îndeplinire
a obligaţiilor prevăzute la art. 5, se interzic:
a) comercializarea produselor
cosmetice a căror formulă finală, pentru a îndeplini cerinţele prezentei legi,
a fost testată pe animale folosindu-se o metodă, alta decât cea alternativă,
după ce aceasta din urmă a fost validată şi adoptată la nivelul Uniunii
Europene, ţinându-se seama de evoluţia procesului de validare din cadrul
Organizaţiei pentru Cooperare şi Dezvoltare Economică;
b) comercializarea produselor cosmetice având
ingrediente sau combinaţii de ingrediente care, pentru a îndeplini cerinţele
prezentei legi, au fost testate pe animale folosindu-se o metodă, alta decât
cea alternativă, după data la care aceasta din urmă a fost validată şi adoptată
la nivelul Uniunii Europene, ţinându-se seama de evoluţia procesului de
validare din cadrul Organizaţiei pentru Cooperare şi Dezvoltare Economică;
c) testarea pe animale a produselor cosmetice finite,
pentru a îndeplini cerinţele prezentei legi;
d) testarea pe animale a ingredientelor sau
combinaţiilor de ingrediente, pentru a îndeplini cerinţele prezentei legi, nu
mai târziu de data la care aceste teste trebuie să fie înlocuite cu una sau mai
multe dintre metodele validate prevăzute în Regulamentul (CE) nr. 440/2008 al Comisiei
din 30 mai 2008 de stabilire a metodelor de testare în temeiul Regulamentului
(CE) nr. 1.907/2006 al Parlamentului European şi al Consiliului privind
înregistrarea, evaluarea, autorizarea şi restricţionarea substanţelor chimice
(REACH).
(2) Metodele prevăzute în anexa nr. IX „Lista metodelor alternative validate de înlocuire a
experimentelor pe animale" la Directiva Consiliului 76/768/CEE din 27
iulie 1976 privind apropierea legislaţiilor statelor
membre cu privire la produsele cosmetice sunt reglementate prin ordin al
ministrului sănătăţii, pe măsura publicării lor în Jurnalul Oficial al Uniunii
Europene.
(3) In situaţii excepţionale,
atunci când există un motiv întemeiat în ceea ce priveşte siguranţa unui
ingredient cosmetic existent, Ministerul Sănătăţii poate solicita Comisiei
Europene să acorde o derogare de la prevederile alin. (1). Cererea de derogare
trebuie să conţină o evaluare a situaţiei şi să indice măsurile necesare. Pe
baza cererii şi după consultarea Comitetului Ştiinţific pentru Cosmetice şi
Produse Nealimentare, Comisia Europeană poate autoriza derogarea prin decizie
motivată. Această autorizare trebuie să conţină condiţiile în care s-a acordat
derogarea, obiectivul specific, durata şi raportarea rezultatelor.
(4) Derogarea poate fi acordată numai dacă:
a) ingredientul se foloseşte în
mod frecvent şi nu poate fi înlocuit de un alt ingredient cu funcţie similară;
b) problema de sănătate umană specifică este
fundamentată şi nevoia de a recurge la testări pe animale este justificată şi
susţinută de un protocol de cercetare detaliat, propus ca bază de evaluare.
Art. 9. - (1) Este permisă comercializarea produselor
cosmetice care conţin:
a) substanţele prevăzute în
anexa nr. III, Partea a 2-a, la Ordinul ministrului sănătăţii nr. 1.448/2005, cu
modificările şi completările ulterioare, în limitele şi condiţiile impuse, până
la data stabilită în anexa menţionată;
b) agenţii de colorare prevăzuţi în anexa nr. IV, Partea a 2-a, la Ordinul ministrului
sănătăţii nr. 1.448/2005, cu modificările şi completările ulterioare, în
limitele şi condiţiile impuse, până la data stabilită în anexa menţionată;
c) conservanţii prevăzuţi în
anexa nr. VI, Partea a 2-a, la
Ordinul ministrului sănătăţii nr. 1.448/2005, cu modificările şi completările
ulterioare, în limitele şi condiţiile impuse, până la data stabilită în anexă,
cu excepţia cazului în care sunt folosite alte concentraţii, pentru scopuri
specifice, care reies din prezentarea produsului;
d) filtrele UV prevăzute în
anexa nr. VII, Partea a 2-a, la Ordinul ministrului sănătăţii nr. 1.448/2005,
cu modificările şi completările ulterioare, în limitele şi condiţiile impuse,
până la data stabilită în anexa menţionată.
(2) După expirarea datei stabilite potrivit alin. (1),
substanţele, agenţii de colorare, conservanţii şi filtrele UV trebuie:
a) permişi definitiv; sau
b) interzişi definitiv, prin includerea în cuprinsul
anexei nr. II la Ordinul ministrului sănătăţii nr. 1.448/2005, cu modificările
şi completările ulterioare; sau
c) menţinuţi, pentru perioada
prevăzută în Partea a 2-a a anexelor nr. III, IV, VI şi VII la Ordinul ministrului sănătăţii nr. 1.448/2005, cu
modificările şi completările ulterioare; sau
d) eliminaţi, prin abrogarea poziţiilor respective din
anexele la Ordinul ministrului sănătăţii nr. 1.448/2005, cu modificările şi
completările ulterioare, pe baza informaţiilor ştiinţifice disponibile sau
pentru că nu mai sunt folosiţi.
Art. 10. - (1) Prin derogare de la prevederile art. 7,
Ministerul Sănătăţii poate autoriza folosirea pe
teritoriul României a substanţelor care nu sunt prevăzute în lista de substanţe
permise pentru anumite produse cosmetice, în următoarele condiţii:
a) autorizarea trebuie să se
limiteze la o perioadă maximă de 3 ani;
b) să se efectueze o verificare
oficială a produselor cosmetice care conţin substanţa sau amestecul a cărui
utilizare a fost autorizată;
c) produsul cosmetic astfel
fabricat trebuie să poarte o indicaţie distinctă, care va fi precizată în
autorizaţie.
(2) Ministerul Sănătăţii
trebuie să informeze Comisia Europeană şi statele membre despre decizia de
autorizare luată conform alin. (1), în decurs de două luni de la data intrării
în vigoare a autorizaţiei.
(3) Inainte de expirarea termenului de 3 ani, prevăzut la alin. (1) lit. a), Ministerul Sănătăţii poate înainta
Comisiei Europene o cerere pentru includerea pe lista substanţelor permise a
substanţei care a primit autorizarea naţională, conform alin. (1). Concomitent,
va comunica documentaţia pe care se întemeiază această cerere şi va indica
utilizările cărora le este destinată substanţa.
Art. 11. - Producătorul sau reprezentantul său
autorizat ori beneficiarul fabricării produsului cosmetic sau persoana
responsabilă pentru punerea produselor cosmetice pe piaţa Uniunii Europene va
notifica autorităţii competente a statului membru unde s-a fabricat produsul
sau unde acesta a fost importat pentru prima dată adresa locului de fabricaţie
ori a primului import în cadrul comunităţii, înainte de introducerea pe piaţă a
acestora.
Art. 12. - (1) Notificarea este unică pe teritoriul
Uniunii Europene.
(2) Notificarea devine efectivă
din momentul transmiterii datelor.
(3) Orice modificare a
informaţiilor transmise Ministerului Sănătăţii este adusă la cunoştinţă
acestuia în termen de 30 de zile de la data apariţiei modificării.
(4) In conformitate cu prevederile art. 11, Ministerul
Sănătăţii reprezintă autoritatea competentă în România pentru notificarea
produselor cosmetice.
Art. 13. - (1) In scopul exercitării controlului de
către autorităţile competente producătorul, reprezentantul său autorizat,
beneficiarul fabricării produsului cosmetic sau persoana responsabilă pentru
punerea pe piaţă a unui produs cosmetic importat trebuie să deţină la adresa
specificată pe etichetă următoarele date:
a) compoziţia calitativă şi cantitativă a produsului;
informaţiile privind compoziţia parfumată şi parfumurile sunt limitate la
numele şi la numărul de cod ale compoziţiei, precum şi la identitatea
furnizorului;
b) specificaţiile
fizico-chimice şi microbiologice pentru materiile prime şi produsul finit şi
criteriile de control de puritate şi microbiologie pentru produsul cosmetic;
c) metoda de fabricaţie conform
regulilor de bună practică de fabricaţie prevăzute în Ordinul ministrului
industriei şi resurselor nr. 308/2001 pentru aprobarea Ghidului privind
principiile de bună practică de fabricaţie pentru produsele cosmetice sau în
reglementările altor state membre; prevederile ordinului menţionat sunt
aplicabile produselor cosmetice fabricate în România sau importate din ţări
terţe, care sunt introduse pentru prima dată pe piaţa comunitară prin România;
d) numele persoanei responsabile cu fabricarea sau
importul pentru prima dată al unui produs cosmetic în Uniunea Europeană;
persoana responsabilă trebuie să posede un nivel adecvat de calificare
profesională sau experienţă, în conformitate cu legislaţia şi practica statului
membru al Uniunii Europene unde sunt fabricate ori unde sunt pentru prima dată
importate produsele cosmetice;
e) evaluarea siguranţei pentru
sănătatea umană a produsului cosmetic finit. Pentru aceasta, producătorul va
ţine seama de profilul toxicologic general al ingredientelor folosite, de
structura lor chimică şi de nivelul de expunere, în special de caracteristicile
de expunere specifice zonei în care produsul va fi aplicat sau de populaţia
căreia îi este destinat; pentru produsele destinate copiilor sub 3 ani, precum
şi pentru cele destinate exclusiv igienei intime externe trebuie să existe o
evaluare specifică a securităţii pentru sănătatea umană. In cazul în care
produsul se fabrică în diferite localităţi pe teritoriul României sau al celorlalte state membre
ale Uniunii Europene, producătorul poate să aleagă o singură locaţie (loc),
unde informaţiile privind produsul sunt disponibile. In acest sens, la
solicitarea autorităţilor competente pentru monitorizarea produsului sau a
altor autorităţi cu atribuţii de control, producătorul este obligat să
precizeze adresa la care informaţiile sunt rapid accesibile;
f) numele şi adresa persoanelor calificate responsabile
care au evaluat produsul din punctul de vedere al siguranţei pentru sănătatea
umană; persoanele responsabile pentru evaluare trebuie să aibă diplomă de
studii superioare în specialităţile: farmacie, toxicologie, dermatologie,
medicină sau o specialitate similară, aşa cum este definită în cuprinsul Legii
nr. 200/2004 privind recunoaşterea diplomelor şi calificărilor profesionale
pentru profesiile reglementate din România, cu modificările şi completările
ulterioare;
g) datele existente cu privire
la efectele nedorite pentru sănătatea umană, provocate de produsele cosmetice
ca urmare a utilizării;
h) dovada privind efectul declarat al produsului
cosmetic, în cazul în care natura acestuia o justifică;
i) informaţii privind orice testări pe animale,
efectuate de producător, agenţii sau furnizorii săi, legate de dezvoltarea
produsului sau de evaluarea siguranţei produsului cosmetic ori a ingredientelor
sale, inclusiv orice testare pe animale, efectuată în scopul respectării unor
reglementări naţionale din ţările care nu sunt membre ale Uniunii Europene.
(2) Autoritatea Naţională pentru Protecţia
Consumatorilor este autoritatea competentă în România pentru verificarea
datelor prevăzute la alin. (1).
(3) Fără a se aduce prejudicii protejării secretului
comercial şi proprietăţii intelectuale, producătorul, reprezentantul său
autorizat, beneficiarul fabricării produsului cosmetic sau persoana
responsabilă cu introducerea pe piaţă a unui produs cosmetic importat va
asigura ca informaţia prevăzută la alin. (1) lit. a) şi g) să fie accesibilă
publicului în orice format, inclusiv electronic. Informaţiile referitoare la
compoziţia cantitativă prevăzută la alin. (1) lit. a) vor fi limitate la
substanţele care îndeplinesc criteriile pentru oricare dintre următoarele clase
sau categorii de pericol prevăzute în anexa nr. I la Regulamentul (CE) nr. 1.272/2008 al Parlamentului European şi al
Consiliului din 16 decembrie 2008 privind clasificarea, etichetarea şi
ambalarea substanţelor şi a amestecurilor, de modificare şi de abrogare a
directivelor 67/548/CEE şi 1999/45/CE, precum şi de modificare a Regulamentului
(CE) nr. 1.907/2006:
a) clasele de pericol 2.1-2.4, 2.6 şi 2.7, 2.8 tipurile
A şi B, 2.9, 2.10, 2.12, 2.13 categoriile 1 şi 2, 2.14 categoriile 1 şi 2, 2.15 tipurile A-F;
b) clasele de pericol 3.1-3.6, 3.7 - efecte adverse asupra funcţiei sexuale şi a fertilităţii sau asupra
dezvoltării, 3.8 - alte efecte decât efectele narcotice, 3.9 şi 3.10;
c) clasa de pericol 4.1;
d) clasa de pericol 5.1.
(4) Evaluarea siguranţei pentru
sănătatea umană, aşa cum este prevăzută la alin. (1) lit. e), va fi efectuată
în conformitate cu principiile de bună practică de laborator prevăzute de
Hotărârea Guvernului nr. 63/2002 privind aprobarea Principiilor de bună
practică de laborator, precum şi inspecţia şi verificarea respectării acestora
în cazul testărilor efectuate asupra substanţelor chimice, cu modificările şi
completările ulterioare.
Art. 14. - Datele prevăzute la art. 13 vor fi
prezentate în mod obligatoriu în limba română, fără a exclude prezentarea şi
într-o limbă acceptată de autorităţile competente.
Art. 15. -In urma efectuării acţiunii de verificare
întreprinse de reprezentanţii împuterniciţi ai organelor de control abilitate,
producătorul, reprezentantul său autorizat, beneficiarul fabricării produsului
cosmetic sau persoana responsabilă pentru punerea pe piaţă a unui produs cosmetic importat, după caz, este obligat să
asigure accesul acestora la datele prevăzute la art. 13, în cel mult 72 de ore
de la solicitare.
Art. 16. - (1) Produsele cosmetice pot fi puse pe piaţă
numai dacă pe recipient şi pe ambalaj informaţiile următoare sunt
inscripţionate vizibil, lizibil şi cu caractere care nu se şterg uşor; în ceea
ce priveşte informaţiile prevăzute la lit. i), acestea pot fi inscripţionate
doar pe ambalaj. Se vor indica următoarele date:
a) numele sau denumirea
producătorului ori a persoanei responsabile cu introducerea pe piaţă stabilite
în Uniunea Europeană sau abrevierea, dacă aceasta permite identificarea
persoanelor respective;
b) sediul sau adresa din statul membru al Uniunii Europene a producătorului sau a persoanei responsabile pentru
introducerea pe piaţă, în Uniunea Europeană, a unui produs cosmetic importat
ori abrevierea sa, atât timp cât acesta este posibil de identificat;
c) ţara de origine pentru produsele fabricate în afara Uniunii Europene;
d) conţinutul nominal în
momentul ambalării produsului, indicat în greutate sau în volum, exceptând
ambalajele ce conţin mai puţin de 5 grame sau mai puţin de 5 mililitri,
eşantioanele gratuite şi dozele unice. In ceea ce priveşte ambalajele în care
se comercializează produse într-un ansamblu de bucăţi şi pentru care indicarea
greutăţii sau a volumului nu este semnificativă, conţinutul poate să nu fie
indicat, dar se va menţiona pe ambalaj numărul de bucăţi; această menţiune nu
este necesară atunci când numărul de piese este uşor de determinat din exterior
sau dacă produsul este comercializat în mod uzual ca unitate;
e) data de minimă durabilitate indicată prin sintagma
„A se folosi preferabil
înainte de ...", urmată de dată sau de indicarea locului de pe ambalaj
unde se află inscripţionată această dată. Data trebuie clar menţionată,
indicându-se, în ordine şi cu cifre arabe, fie luna şi anul, fie ziua, luna şi
anul. Dacă este necesar, această informaţie va fi suplimentată de o indicare a
condiţiilor care trebuie îndeplinite pentru a se garanta durabilitatea
afirmată. Indicarea datei de durabilitate nu este obligatorie pentru produsele
cosmetice a căror durabilitate minimă depăşeşte 30 de luni. Pentru acestea
menţiunile se completează cu indicarea perioadei, după deschiderea produsului
cosmetic, în care poate fi folosit în siguranţă de către consumatori. Această
informaţie va fi redată prin simbolul prevăzut în anexa nr. 2, urmat de perioada
de utilizare exprimată în luni şi/sau ani;
f) precauţiile speciale la
utilizare, în special cele referitoare la ingredientele menţionate în coloana
„Condiţiile utilizării şi precauţii care trebuie să fie menţionate pe
etichetă" din anexele nr. III, IV, VI şi VII la Ordinul ministrului sănătăţii nr. 1.448/2005, cu
modificările şi completările ulterioare, şi care trebuie inscripţionate pe
ambalaj şi pe recipient, precum şi informaţiile speciale de avertizare pentru
produsele cosmetice de uz profesional, în special cele pentru coafură. In cazul
în care acest lucru nu este posibil din motive practice, va fi alăturat un
prospect, o etichetă, o banderolă ori un fluturaş care va conţine informaţiile
necesare consumatorilor, fie abreviat, fie prin utilizarea simbolului prevăzut
în anexa nr. 3, care trebuie să figureze pe recipient şi pe ambalaj;
g) funcţia produsului cosmetic,
exceptând cazul în care aceasta rezultă din prezentarea produsului;
h) numărul lotului de fabricaţie sau o indicaţie care
să permită identificarea produsului. Atunci când dimensiunile reduse ale
produsului nu permit, această informaţie poate să apară numai pe ambalaj;
i) lista cuprinzând ingredientele care fac parte din
compoziţia produsului cosmetic, în ordinea descrescătoare a greutăţii în
momentul încorporării lor; această listă este precedată de cuvântul
„ingrediente". In cazul în care, din motive practice, acest lucru nu este
posibil, prospectul, eticheta, banderola sau fluturaşul ataşat trebuie să
conţină informaţia necesară consumatorului, în forma abreviată sau simbolul
prevăzut în anexa nr. 3, care trebuie inscripţionat pe ambalaj. Nu sunt
considerate ingrediente: impurităţile din materiile prime folosite; materialele
tehnice auxiliare folosite în amestec, dar care nu se regăsesc în produsul
finit; materialele folosite în cantităţi strict necesare ca solvenţi sau
purtători de parfum ori compoziţii aromatice. Se vor menţiona ingredientele în
concentraţie mai mică de 1% fără o ordine anume, după cele a căror concentraţie
este mai mare de 1%. Coloranţii pot fi menţionaţi după celelalte ingrediente,
indiferent de ordine, conform numărului index de culoare sau denumirii
prevăzute în anexa nr. VI la Ordinul ministrului sănătăţii nr. 1.448/2005, cu
modificările şi completările ulterioare. Pentru produsele cosmetice decorative
comercializate în mai multe culori/nuanţe se menţionează toţi agenţii de
colorare folosiţi, precedaţi de sintagma „poate conţine" sau de simbolul
„+/-". Compoziţiile de parfumare sau de aromatizare şi materiile lor prime
vor fi menţionate prin cuvântul „parfum", respectiv „aromă."
Substanţele cuprinse în anexa nr. III la Ordinul ministrului sănătăţii nr.
1.448/2005, cu modificările şi completările ulterioare, pentru care există
menţiunea de a fi inscripţionate pe ambalaj, vor fi incluse pe lista
ingredientelor, indiferent de funcţiunea pe care o au în produsul cosmetic.
(2) Acolo unde, din motive practice legate de
dimensiunea sau de forma recipientelor ori a ambalajelor, nu este realizabilă
inscripţionarea informaţiilor prevăzute la alin. (1) lit. f) şi i), acestea se
înscriu pe o etichetă, o banderolă, un prospect sau un pliant care este
alăturat produsului. In cazul săpunului, al bilelor pentru baie sau al altor
produse de dimensiuni mici, unde este practic imposibil, din motive de
dimensiune sau formă, să fie scrise informaţiile prevăzute la alin. (1) lit. i)
pe un prospect, o etichetă, o banderolă, un pliant sau un fluturaş ataşat,
aceste informaţii vor fi scrise pe un pliant pus în imediata vecinătate a
recipientului în care produsul cosmetic este expus spre vânzare.
(3) Pentru produsele cosmetice
care nu sunt preambalate şi care sunt ambalate la punctul de vânzare la cererea
cumpărătorului ori care sunt preambalate pentru imediata vânzare, regulile
detaliate pentru modul de indicare a informaţiilor prevăzute la alin. (1) se
aprobă prin ordin al ministrului sănătăţii, care se publică în Monitorul
Oficial al României, Partea I.
Art. 17. - Informaţiile prevăzute la art. 16 alin. (1)
lit. d)-f) şi h) trebuie scrise în limba română, cu excepţia listei cuprinzând
ingredientele, unde se folosesc denumirile din Ordinul ministrului industriei
şi resurselor şi al ministrului sănătăţii şi familiei nr. 309/729/2001 ori din
Nomenclatorul internaţional pentru produse cosmetice - INCI, afişat pe site-ul
Ministerului Sănătăţii şi pe cel al Uniunii Europene, sau, după caz, se aplică
prevederile cuprinse în Hotărârea Guvernului nr. 560/2001*) privind unele
măsuri pentru păstrarea confidenţialităţii unor ingrediente din compoziţia produselor
cosmetice, iar coloranţii vor fi înscrişi conform numărului din indexul
culorilor - Colour Index.
*) Hotărârea Guvernului nr. 560/2001 a fost abrogată
prin Hotărârea Guvernului nr. 562/2008 privind unele măsuri pentru păstrarea
confidenţialităţii unor ingrediente din compoziţia produselor cosmetice,
publicată în Monitorul Oficial al României, Partea I, nr. 417 din 3 iunie 2008.
Art. 18. - (1) Ministerul Sănătăţii nu poate interzice,
restrânge sau împiedica introducerea pe piaţă a produselor cosmetice care
îndeplinesc cerinţele prevăzute de prezenta lege.
(2) In vederea asigurării unui tratament medical prompt
şi adecvat în cazul unor situaţii cu risc pentru sănătate, la solicitarea
Ministerului Sănătăţii, producătorul, importatorul sau persoana responsabilă cu
introducerea pe piaţă trebuie să asigure furnizarea informaţiilor necesare şi
adecvate privind substanţele folosite în produsele cosmetice.
(3) Ministerul Sănătăţii este autoritatea naţională
competentă care asigură transmiterea informaţiilor prevăzute la alin. (2) către
oricare dintre statele membre ale Uniunii Europene, la solicitarea acestora,
luând măsurile necesare pentru ca informaţia să fie transmisă doar în scopul
aplicării unui tratament medical adecvat.
Art. 19. - (1) In etichetare, prezentarea spre vânzare
sau promovarea produsului se interzice întrebuinţarea
textelor, denumirilor, mărcilor, imaginilor sau a altor însemne care atribuie
produselor caracteristici pe care acestea nu le au.
(2) Producătorul sau persoana responsabilă cu plasarea
pe piaţa Uniunii Europene a produsului se poate folosi de faptul că acesta nu a
fost testat pe animale, prin specificare pe ambalaj sau pe orice alt document,
notă, etichetă, banderolă ce însoţeşte ori care se referă la produs, numai dacă
producătorul sau furnizorii săi de materii prime nu a/au efectuat sau nu a/au
solicitat testări pe animale pentru produsul cosmetic finit ori pe prototip sau
nu a/au folosit niciun ingredient testat pe animale de către terţe persoane, în
scopul formulării de produse cosmetice noi.
CAPITOLUL III
Sancţiuni
Art. 20. - Incălcarea prevederilor prezentei legi
atrage răspunderea materială, civilă, contravenţională sau penală, după caz.
Art. 21. - Constituie contravenţii şi se sancţionează
cu amendă următoarele fapte:
a) nerespectarea prevederilor art. 13, 14 si 17, cu
amendă de la 1.000 lei la 2.000 lei;
b) nerespectarea prevederilor art. 15, 16 si 19, cu
amendă de la 2.000 lei la 3.000 lei;
c) nerespectarea prevederilor art. 5, 7, 8, 11, art. 18
alin. (2) şi art. 23, cu amendă de la 5.000 lei la 10.000 lei.
Art. 22. - (1) Constatarea
contravenţiilor şi aplicarea sancţiunilor prevăzute la art. 21 se fac de către
reprezentanţii împuterniciţi ai Autorităţii Naţionale pentru Protecţia
Consumatorilor şi ai Ministerului Sănătăţii.
(2) Organele de control abilitate potrivit alin. (1) pot dispune justificat oprirea temporară sau definitivă a fabricării
şi/sau a punerii pe piaţă a produselor cosmetice care nu corespund cerinţelor
prezentei legi şi care pot afecta viaţa sau sănătatea consumatorilor.
(3) Organele de control pot preleva probe de produs cosmetic pe care le consideră necesare, în vederea
efectuării de analize.
Art. 23. -In cazul în care Ministerul Sănătăţii
constată, pe baza unor dovezi întemeiate, că un produs cosmetic, deşi respectă
cerinţele prezentei legi, reprezintă un pericol pentru sănătate, poate
interzice provizoriu comercializarea acelui produs sau poate impune condiţii
speciale pentru comercializarea acestuia pe teritoriul României. In acest caz, va informa imediat Comisia Europeană şi
statele membre ale Uniunii Europene asupra acestei decizii şi asupra motivelor
care au fundamentat această decizie.
Art. 24. - Reprezentanţii împuterniciţi ai organelor de
control sunt obligaţi să respecte caracterul secret al informaţiilor conţinute
în documentele prevăzute la art. 13 sau despre care au luat cunoştinţă în
timpul acţiunilor de control.
Art. 25. - (1) Ministerul Sănătăţii este autoritatea
naţională competentă care transmite informaţii Comisiei Europene referitoare la
dispoziţiile art. 13, în scopul publicării în Jurnalul Oficial al Uniunii Europene.
(2) Ministerul Sănătăţii asigură cooperarea cu
autorităţile competente ale statelor membre, pentru aplicarea dispoziţiilor
prezentei legi.
Art. 26. -In cazul în care Ministerul Sănătăţii a
decis, potrivit art. 23, interzicerea provizorie sau restricţionarea
comercializării unui produs cosmetic, acesta informează în scris, în termen de
72 de ore, partea interesată/implicată despre această măsură, indicând motivele
deciziei şi măsurile de remediere recomandate, în conformitate cu
reglementările legale existente, precum şi data-limită până la care acestea pot
fi aplicate.
Art. 27. - Prevederile art. 21 se completează cu
dispoziţiile Ordonanţei Guvernului nr. 2/2001 privind regimul juridic al
contravenţiilor, aprobată cu modificări şi completări prin Legea nr. 180/2002,
cu modificările şi completările ulterioare.
CAPITOLUL IV
Dispoziţii finale
Art. 28. - Ministerul Sănătăţii va stabili, până la
data de 31 decembrie 2006, procedura prin care unele substanţe şi amestecuri
chimice pot fi autorizate temporar, pentru a fi utilizate în produsele
cosmetice, mecanismul de acces la informaţiile despre substanţele folosite în
fabricarea produselor cosmetice necesare pentru asigurarea tratamentelor
medicale adecvate în cazul unor situaţii cu risc pentru sănătate, care se
aprobă prin ordin al ministrului sănătăţii.
Art. 29. - Prevederile prezentei legi nu se aplică
produselor care conţin substanţele prevăzute în anexa nr. V la Ordinul ministrului sănătăţii nr.
1.448/2005, cu modificările şi completările ulterioare.
Art. 30. - (1) Prezenta lege intră în vigoare la 60 de
zile de la publicarea ei în Monitorul Oficial al României, Partea I*).
(2) Pe data intrării în vigoare a prezentei legi se
abrogă:
a) pct. 21 şi 22 din anexa nr.
2 la Hotărârea Guvernului nr. 340/1992 privind regimul de import al deşeurilor
şi reziduurilor de orice natură, precum şi al altor mărfuri periculoase pentru
sănătatea populaţiei şi pentru mediul înconjurător, republicată în Monitorul
Oficial al României, Partea I, nr. 201 din 18 august 1992, cu modificările şi completările ulterioare;
b) dispoziţiile referitoare la
înregistrarea produselor cosmetice cuprinse în art. 4 lit. b) din Ordonanţa
Guvernului nr. 125/1998 privind înfiinţarea, organizarea şi funcţionarea
Agenţiei Naţionale a Medicamentului, publicată în Monitorul Oficial al
României, Partea I, nr. 329
din 31 august 1998, cu modificările ulterioare;
c) Hotărârea Guvernului nr.
670/2001 pentru aprobarea Normelor metodologice de aplicare a Legii nr.
178/2000 privind produsele cosmetice, publicată în Monitorul Oficial al
României, Partea I, nr. 422 din 30 iulie 2001;
d) orice alte dispoziţii contrare.
Art. 31. -Anexele nr. 1-3 fac parte integrantă din prezenta
lege.
*) Legea nr. 178/2000 a fost publicată în Monitorul
Oficial al României, Partea I, nr. 525 din 25 octombrie
2000.
ANEXA Nr. 1
LISTA
cuprinzând categoriile de produse cosmetice
- Creme, emulsii, loţiuni, geluri şi uleiuri pentru
piele (mâini, faţă, picioare etc.)
- Măşti pentru faţă (cu excepţia produselor care
acţionează ca abrazive superficiale ale pielii pe cale chimică)
- Baze nuanţatoare (lichide, paste, pudre etc.)
- Pudre de machiaj, pudre după baie, pudre igienice
etc.
- Săpunuri de toaletă, săpunuri deodorante etc.
- Parfumuri, ape de toaletă, ape de colonie etc.
- Amestecuri pentru baie şi duş (săruri, spume,
uleiuri, geluri etc.)
- Depilatoare
- Deodorante şi antiperspirante
- Produse pentru îngrijirea părului:
- nuanţatoare şi decolorante;
- produse pentru ondulare, îndreptare şi fixare;
- produse pentru aranjare (decorare);
- produse pentru curăţare (loţiuni, pudre, şampoane
etc);
- produse de condiţionare (loţiuni, creme, uleiuri
etc);
- produse de coafare (loţiuni, lacuri, briantine etc);
- Produse pentru ras (creme, spume, loţiuni etc.)
- Produse pentru machiaj şi
îndepărtarea acestuia de pe faţă şi ochi
- Produse destinate aplicării pe buze
- Produse pentru îngrijirea dinţilor şi a gurii
- Produse pentru îngrijirea unghiilor şi decorarea lor
- Produse pentru igiena intimă externă
- Produse pentru băi de soare
(plajă)
- Produse pentru bronzare fără soare
- Produse de albire a pielii
- Produse antirid.
ANEXA Nr. 2*)
Simbolul pentru indicarea perioadei după deschidere
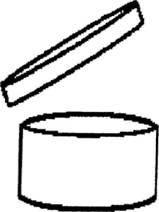
*) Anexa nr. 2 este reprodusă în facsimil.
ANEXA Nr. 3*)
Simbolul pentru precauţiunile
particulare de utilizare

*) Anexa nr. 3 este reprodusă în facsimil.
NOTĂ:
Reproducem mai jos prevederi care nu sunt încorporate
în forma republicată a Legii nr. 178/2000 şi care se aplică, în continuare, ca
dispoziţii proprii ale actelor modificatoare:
1. Menţiunea transpunerii din
Legea nr. 469/2006 pentru modificarea şi completarea Legii nr. 178/2000 privind
produsele cosmetice:
„Prezenta lege transpune integral Directiva Consiliului
76/768/CEE privind armonizarea legislaţiilor statelor membre în domeniul
produselor cosmetice, publicată în Jurnalul Oficial al Comunităţilor Europene
nr. L/262 din 27 septembrie 1976."
2. Art. II şi menţiunea
transpunerii din Ordonanţa Guvernului nr. 2/2010 pentru modificarea Legii nr.
178/2000 privind produsele cosmetice, aprobată prin Legea nr. 159/2010:
„Art. II. - Dispoziţiile
prezentei ordonanţe intră în vigoare la data de 1 iunie 2010, cu excepţia
dispoziţiilor art. I pct. 2 şi 3 care intră în vigoare la data de 1 decembrie
2010.
*
Prezenta ordonanţă transpune art. 1 «Modificări ale
Directivei 76/768/CEE» din Directiva 2008/112/CE a Parlamentului European şi a
Consiliului din 16 decembrie 2008 de modificare a
directivelor 76/768/CEE, 88/378/CEE, 1999/13/CE ale
Consiliului şi a directivelor 2000/53/CE, 2002/96/CE şi 2004/42/CE ale
Parlamentului European şi ale Consiliului, pentru a le adapta Regulamentului
(CE) nr. 1.272/2008 privind clasificarea, etichetarea şi ambalarea substanţelor
şi a amestecurilor, publicată în Jurnalul Oficial al Uniunii Europene nr. L 345 din 23 decembrie 2008."
3. Art. I şi II din Legea nr. 260/2010 pentru abrogarea art. 8 din Legea nr.
178/2000 privind produsele cosmetice:
„Art. I. -Articolul 8 din Legea
nr. 178/2000 privind produsele cosmetice, republicată în Monitorul Oficial al României, Partea I, nr. 91 din 27 ianuarie
2005, cu modificările şi completările ulterioare, se abrogă.
Art. II. -In cuprinsul actelor
normative, trimiterile la art. 8 din Legea nr. 178/2000, republicată, cu
modificările şi completările ulterioare, se interpretează ca trimiteri la
prevederile art. 15 alin. (1) şi (2) din Regulamentul (CE) nr. 1.223/2009 al
Parlamentului European şi al Consiliului din 30 noiembrie 2009 privind
produsele cosmetice, publicat în Jurnalul Oficial al Uniunii Europene nr. L 342
din 22 decembrie 2009, precum şi la art. 14, 31 şi 32 din acelaşi regulament,
în cazul în care acestea sunt necesare pentru aplicarea prevederilor art. 15
alin. (1)şi (2)."